题目内容
6.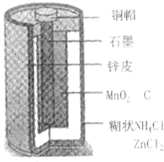 Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.(1)该电池的负极材料是Zn.电池工作时,电子从Zn极流向正极(填“正极”或“负极”).
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是Zn+Cu2+=Zn2++Cu,形成原电池发生反应.欲除去Cu2+,最好选用下列试剂中的B(填代号).
A.NaOH B.Zn C.Fe D.NH3•H2O
(3)MnO2的生产方法之一是以惰性电极电解MnCl2和HCl混合溶液,请问MnO2在阳极产生.阳极的电极反应式是:Mn2++2H2O-2e-=MnO2+4H+.若电解电路中通过2mol电子,MnO2的理论产量为87g.(MnO2的摩尔质量为:87g/mol)
分析 (1)锌锰原电池中负极材料为活泼金属Zn,MnO2为正极,电池工作时电子从负极经外电路流向正极;
(2)锌比铜活泼,能置换出铜形成原电池加速锌的腐蚀,除杂时注意不能引入新的杂质;
(3)以石墨为电极,电解酸化的MnSO4溶液,阳极锰离子放电;结合转移的电子及电极反应计算.
解答 解:(1)Zn-MnO2干电池中,活泼金属锌做原电池的负极,工作时原电池中电子从负极经外电路流向电源的正极,故答案为:Zn;正极;
(2)锌比铜活泼,能置换出铜,反应为Zn+Cu2+=Zn2++Cu,形成原电池加速锌的腐蚀,除杂时注意不能引入新的杂质只有B符合,
故答案为:Zn+Cu2+=Zn2++Cu,形成原电池发生反应;B;
(3)以石墨为电极,电解酸化的MnSO4溶液,阳极锰离子放电,阳极反应为Mn2+-2e-+2H2O=MnO2+4H+;通过2mol电子,MnO2的理论产量为1mol×87g/mol=87g,
故答案为:阳;Mn2++2H2O-2e-=MnO2+4H+;87.
点评 本题是将典型的实验知识与原电池原理、电解原理相融合的题型,涉及了电极材料分析、电解液净化及相关电化学计算等内容,具有较宽的知识覆盖面.学习中要电化学基础知识掌握扎实.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
17.下列叙述正确的是( )
| A. | 在一定条件下通入氢气发生反应,可除去乙烷中混有的乙烯 | |
| B. | 苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴 | |
| C. |  的一氯代物有4种 的一氯代物有4种 | |
| D. | 甲醛溶液与足量的银氨溶液共热的离子反应方程式为:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |
14.链式炔碳…-C≡C-C≡C-C≡C…是现已发现的碳的第四种同素异形体,已知链式炔碳C300经过适当的处理可得含多个-C≡C-(不含-C≡C-)的链状化合物C300H302,则该分子中含-C≡C-的数目为( )
| A. | 73 | B. | 74 | C. | 75 | D. | 76 |
1.在一定温度下,可逆反应X(g)+3Y(g)?2Z(g)达到平衡的标志是( )
| A. | X、Y、Z的浓度不再变化 | |
| B. | 单位时间生成a mol X,同时生成3a mol Y | |
| C. | X、Y、Z的分子数比为1:3:2 | |
| D. | Z生成的速率与X生成的速率相等 |
11.下列离子方程式正确的是( )
| A. | 铁粉加入三氯化铁溶液中 Fe+Fe3+═2Fe2+ | |
| B. | Cl2与水的反应Cl2+H2O═2H++Cl-+ClO- | |
| C. | 铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag | |
| D. | 大理石溶于醋酸的反应CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
18.下列有关实验的说法不正确的是( )
| A. | 测定中和热实验的玻璃仪器只需烧杯、量筒和温度计 | |
| B. | 用25mL碱式滴定管量取13.50mL Na2CO3溶液 | |
| C. | 用10mL量筒量取5.5mL硫酸溶液 | |
| D. | 用广泛pH试纸不能测得某碱溶液的pH为12.7 |
15.已知某有机物的结构简式如图所示,下列说法不正确的是( )
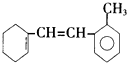
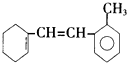
| A. | 分子式为C15H18 | |
| B. | 能使酸性KMnO4溶液褪色,且是氧化反应 | |
| C. | 1mol该物质最多和2molH2加成 | |
| D. | 苯环上的一氯化物有4种 |
16.将ag镁铁合金投入适量稀硝酸(假设NO是唯一的还原产物,不考虑溶解氧等其它氧化剂)中,当硝酸消耗完时收集到标准状况下2.24L的气体.然后向反应后的溶液中加入3mol•L-1NaOH溶液至金属恰好沉淀完全,沉淀质量为bg,则下列说法不正确的( )
| A. | 若在与硝酸反应后的溶液中再加入Fe,金属可能溶解 | |
| B. | 消耗的氢氧化钠的体积为100mL | |
| C. | b=a+5.1 | |
| D. | a的范围为:3.6<a<5.6 |