题目内容
以下属于共价分子的单质是( )
| A、氩气 | B、金刚石 | C、重氢气 | D、水 |
考点:共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:由多原子构成的分子中,只有一种元素组成,则为共价键形成的分子,以此来解答.
解答:
解:A.氩气为单原子构成的分子,不含化学键,故A不选;
B.金刚石为原子晶体,不含分子,故B不选;
C.重氢气中只含D-D共价键,为分子,故C选;
D.水中含H、O元素,为含共价键的共价化合物,故D不选;
故选C.
B.金刚石为原子晶体,不含分子,故B不选;
C.重氢气中只含D-D共价键,为分子,故C选;
D.水中含H、O元素,为含共价键的共价化合物,故D不选;
故选C.
点评:本题考查共价键及物质的类别,为高频考点,把握化学键判断的一般规律及物质的组成为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
已知:H2(g)+
O2(g)=H2O(g)△H=-242kJ/mol,断开1 mol O=O键和1 molH-O键所吸收的能量分别为496 kJ和463kJ,则断开1 mol H-H键所吸收的能量为( )
| 1 |
| 2 |
| A、920 kJ |
| B、557 kJ |
| C、436 kJ |
| D、188 kJ |
下列离子方程式书写正确的是( )
| A、向碳酸钠溶液中滴加与其溶质的物质的量相等的盐酸:CO32-+2H+=CO2↑+H2O |
| B、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、足量铁粉与稀硝酸反应:Fe+4H++NO3-=Fe3++2H2O+NO↑ |
| D、向漂白粉溶液中通入少量二氧化硫:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
下列混合气体在指定条件下可以大量共存的是( )
| A、日光照射下H2和Cl2 |
| B、常温下H2S和SO2 |
| C、常温下H2和F2 |
| D、常温下H2和O2 |
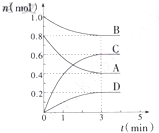 在T℃时,在容积为0.5L的密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)+qD(s),△H<0(m、n、p、q为最简整数比).A、B、C、D物质的量的变化如图所示:
在T℃时,在容积为0.5L的密闭容器中发生如下反应:mA(g)+nB(g)?pC(g)+qD(s),△H<0(m、n、p、q为最简整数比).A、B、C、D物质的量的变化如图所示: