题目内容
(1)3.6克H2O的物质的量是 ,含有 个H2O,含有 molH.
(2)3.01×1023个OH-的物质的量为 ,质量为 ,含有质子的物质的量为 ,含有电子的物质的量为 .
(2)3.01×1023个OH-的物质的量为
考点:物质的量的相关计算
专题:计算题
分析:(1)根据n=
=
计算;
(2)根据n=
=
结合物质的原子构成计算.
| m |
| M |
| N |
| NA |
(2)根据n=
| m |
| M |
| N |
| NA |
解答:
解:(1)水的摩尔质量是18g/mol,所以根据n=m/M可知,3.6g水的物质的量是0.2mol,则根据根据n=
可知,含有的水分子数是0.2mol×6.02×1023/mol=1.204X1023个;水分子是由2个氢原子和1个氧原子构成的,因此含有0.4mol氢原子,
故答案为:0.2mol;1.204×1023;0.4;
(2)根据n=
可知,3.01×1023个OH-的物质的量为3.01×1023÷6.02×1023/mol=0.5mol;
质量是0.5mol×17g/mol=8.5g;
OH-中含有9个质子和10个电子,因此含有质子的物质的量是0.5mol×9=4.5mol,电子的物质的量是0.5mol×10=5mol.
故答案为:0.5mol;8.5g;4.5mol;5mol.
| N |
| NA |
故答案为:0.2mol;1.204×1023;0.4;
(2)根据n=
| N |
| NA |
质量是0.5mol×17g/mol=8.5g;
OH-中含有9个质子和10个电子,因此含有质子的物质的量是0.5mol×9=4.5mol,电子的物质的量是0.5mol×10=5mol.
故答案为:0.5mol;8.5g;4.5mol;5mol.
点评:本题考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意相关计算公式的运用,难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、分子式为C4H8有机物最多存在4个C-C单键 |
B、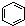 和 和 均是芳香烃, 均是芳香烃, 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 |
C、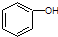 和 和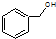 分子组成相差一个-CH2-,因此是同系物关系 分子组成相差一个-CH2-,因此是同系物关系 |
| D、乙酸分子中含有碳氧双键,所以它能使溴水褪色 |
800℃时,焦炭与水蒸气反应生成一氧化碳和氢气,反应热△H=+131.3kJ?mol-1,它表示( )
| A、碳和水反应吸收热量131.3 kJ |
| B、1 mol C(s)和1 mol H2O(g)反应生成一氧化碳和氢气,并吸收131.3 kJ的热量 |
| C、1 mol C跟1 mol H2O反应吸收131.3 kJ的热量 |
| D、固体碳和气态水各1 mol反应,放出131.3 kJ的热量 |
下列选项正确的是( )
 制取氧气 | 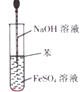 制取Fe(OH)2 |  用盐酸滴定NaOH溶液 |  制备乙酸乙酯 |
| A | B | C | D |
| A、A | B、B | C、C | D、D |
以下属于共价分子的单质是( )
| A、氩气 | B、金刚石 | C、重氢气 | D、水 |
设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温下,46g NO2中含有氧原子个数为2NA |
| B、在标准状况下,22.4 L丙烷中所含C-H键数目为6NA |
| C、将58.5g NaCl溶于1 L水中,溶液中所含Na+和Cl-总数为2NA |
| D、以二氧化锰和浓盐酸为原料制备氯气,当生成1mol氯气,电子转移总数为4NA |
用下列装置不能达到有关实验目的是( )
A、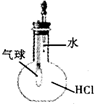 验证HCl的溶解性 |
B、 制备Fe(OH)2 |
C、 干燥并收集NH3 |
D、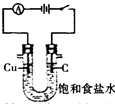 利用电解法制H2和Cl2 |
已知酸H2B在水溶液中存在下列关系:①H2B=H++HB-,②HB-?H++B2-,则下列说法中一定正确的是( )
| A、NaHB溶液可能存在以下关系:c(Na+)>c(HB-)>c(OH-)>c(H+) |
| B、NaHB溶液一定呈酸性,Na2B溶液一定呈碱性 |
| C、NaHB水溶液中一定有:c(Na+)+c(H+)=c(HB-)+c(OH-)+c(B2-) |
| D、在Na2B溶液中一定有:c(OH-)=c(H+)+c(HB-)+2c(H2B) |