题目内容
某气体通入品红溶液中,溶液褪色。加热后又恢复为原来颜色。该气体是
A
【解析】
试题分析:A、 SO2具有漂白性,漂白原理是与某些有机色质结合生成无色物质,该无色物质不稳定,在加热的条件下又恢复到原来的颜色,正确;B、NO2溶于水生成硝酸,具有强氧化性,利用硝酸的强氧化性将有机色质氧化生成稳定无色物质,加热不能恢复原来的颜色,错误;C、CO2不能使品红溶液褪色,错误;D、氯气溶于水生成的次氯酸具有强氧化性,利用次氯酸的强氧化性将有机色质氧化生成稳定无色物质,加热不能恢复原来的颜色,错误。
考点:考查物质漂白性原理以及特点的判断。

(16分)Ⅰ.用中和滴定法测定某烧碱样品的纯度。(锥形瓶中装待测液)配制待测液:将2.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制200mL溶液。
(1)滴定:盛装0.20mol/L盐酸标准液应该用酸式滴定管;滴定时,先向盛待测液的锥形瓶中加酚酞作为指示剂;滴定终点的现象是:_____________________________
(2)有关数据记录如下:
滴定序号 | 待测液体积(ml) | 所消耗盐酸标准液的体积(ml) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.50 | 20.55 |
2 | 20.00 | 6.00 | 25.95 |
纯度计算:烧碱样品的纯度为________________。
(3)对几种假定情况的讨论:(填无影响、偏高、偏低)(测定的结果指烧碱溶液的浓度)
①若用蒸馏水冲洗锥形瓶,则会使测定的结果___________________
②若滴定前用蒸馏水冲洗酸式滴定管后即装标准盐酸,则会使测定结果__________
③滴加盐酸时未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果________。
Ⅱ.现有室温下浓度均为1×10-3 mol/L的几种溶液:①盐酸、②硫酸、③醋酸、④NaOH溶液,回答下列问题:
(1)将③、④混合后,若溶液呈中性,则消耗两溶液的体积为③________④(填“>”、“<”或“=”)。溶液中的离子浓度由大到小的顺序为________________。
(2)向相同体积的①、②、③溶液中分别加入相同的且足量的锌粒,反应的初始速率由快到慢的顺序为___________,(填序号)最终产生H2总量的关系为___________(填序号)
(3)向相同体积的①、③溶液中分别加入相同浓度、相同体积的CH3COONa溶液,充分混合后,混合液的pH大小关系为①_________③(填“>”、“<”或“=”)
(10分)工业上利用电解污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
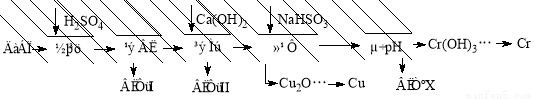
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
Fe3+ | Cu2+ | Cr3+ | |
开始沉淀pH | 2.1 | 4.7 | 4.3 |
完全沉淀pH | 3.2 | 6.7 | a |

(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有 。
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:①加入石灰乳调节pH范围为: ~ ;②将浊液加热到80℃, 。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体的离子反应方程式 ,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是 。
 B.
B.
 D.
D.
 -OH)2用它制成的试纸可以检验溶液的酸碱性。能够跟1 mol该化合物起反应的Br2水溶液或H2的最大用量分别是
-OH)2用它制成的试纸可以检验溶液的酸碱性。能够跟1 mol该化合物起反应的Br2水溶液或H2的最大用量分别是

