题目内容
6.下列有关钠及其化合物的说法正确的是( )| A. | 用手掰开一块金属钠,观察钠的颜色 | |
| B. | 钠投入硫酸铜溶液中,既有气体又有沉淀生成 | |
| C. | 氧化钠和过氧化钠可用作潜艇里氧气的来源 | |
| D. | 氧化钠和过氧化钠与二氧化碳反应的产物完全相同 |
分析 A、钠具有腐蚀性;
B、钠与水硫酸铜反应生成氢气、氢氧化铜沉淀和硫酸钠;
C、过氧化钠与水反应生成氧气,而氧化钠与水反应只生成氢氧化钠;
D、氧化钠与二氧化碳反应生成碳酸钠,而过氧化钠与二氧化碳反应生成碳酸钠与氧气.
解答 解:A、钠具有腐蚀性,不能用手钠取,应用镊子取,用小刀切割,故A错误;
B、钠与水硫酸铜反应生成氢气、氢氧化铜沉淀和硫酸钠,所以既有气体又有沉淀生成,故B正确;
C、过氧化钠与水反应生成氧气,而氧化钠与水反应只生成氢氧化钠,所以氧化钠不能作潜艇里氧气的来源,故C错误;
D、氧化钠与二氧化碳反应生成碳酸钠,而过氧化钠与二氧化碳反应生成碳酸钠与氧气,故D错误;
故选B.
点评 本题考查了常见元素及其化合物性质,题目难度不大,明确钠及其化合物性质为解答关键,注意氧化钠与水和二氧化碳反应不生成氧气.

练习册系列答案
相关题目
16.ICl3遇水会产生大量的腐蚀性白色浓雾,有强烈的催泪性.若两种生成物之一是HCl,则另一种是( )
| A. | HIO3 | B. | HIO2 | C. | HIO | D. | ICl |
14.已知位于同周期的X、Y、Z三元素,它们的最高价氧化物的水化物分别为HXO4、H2YO4、H3ZO4,下列判断不正确的是( )
| A. | 阴离子的还原性:X<Y<Z | B. | 单质的氧化性:X>Y>Z | ||
| C. | 酸性:H3ZO4>H2YO4>HXO4 | D. | 气态氢化物的稳定性:X>Y>Z |
1.一定条件下,将TiO2和焦炭放入密闭真空容器中,反应TiO2(s)+C(s)?Ti(s)+CO2 (g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法一定正确的是( )
| A. | 平衡常数减小 | B. | TiO2的质量不变 | C. | CO2的浓度不变 | D. | Ti的质量增加 |
11.对于溶液中某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄淸石灰水,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入KSCN溶液无明显现象,再加入新制氯水溶液变为血红色,一定有Fe2+ | |
| D. | 加入过量硝酸银溶液,产生白色沉淀,再加入稀盐酸沉淀不溶解,则一定含有C1- |
18.用石墨作电极,电解1mol•L-1下列物质的溶液,通电一段时间后溶液的pH升高的是( )
| A. | H2 SO4 | B. | CuSO4 | C. | Na2 SO4 | D. | NaCl |
15.下列实验操作中错误的是( )
| A. | 用量筒量取12.12mL的盐酸 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 称量时,称量物应放在托盘天平的左盘,砝码放在托盘天平的右盘中 |
1.要使等浓度、等体积的AlCl3、CaCl2、NaCl溶液中的Cl-完全转化为AgCl沉淀,所用0.1mol•L-1AgNO3溶液的体积之比为( )
| A. | 1﹕2﹕3 | B. | 1﹕1﹕1 | C. | 2﹕3﹕6 | D. | 3﹕2﹕1 |
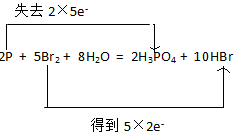 .反应中氧化剂与还原剂的物质的量之比为5:2.
.反应中氧化剂与还原剂的物质的量之比为5:2.