题目内容
15.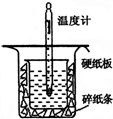 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:(1)从如图实验装置看,其中尚缺少的一种玻璃用品是环形玻璃搅拌棒,除此之外,装置中的一个明显错误是小烧杯口未用硬纸板盖住(或大烧杯内碎纸条塞少了,未将小烧杯垫的足够高).
(2)图中的小烧杯应该选择下列哪种规格的②.(选填代号)
①50mL ②100mL ③150mL ④250mL
(3)为了便于计算,假定混合前后溶液的密度都近似为1g.cm-3,假定反应后生成溶液的比热容近似为水的比热容4.18J.g-1.℃-1,用t1℃和t2℃代表反应前后溶液的温度,则该实验中和热的计算表达式为△H=-$\frac{0.418({t}_{2}{-t}_{1})}{0.025}$kJ/mol.
分析 (1)根据量热计的构造来判断该装置的缺少仪器;为了减少热量的损失,大烧杯杯口与小烧杯杯口相平;
(2)根据混合液总体积判断烧杯的规格;
(3)根据Q=m•c•△T计算出反应放出的热量,然后计算出生成1mol水放出的热量,就可以得到中和热.
解答 解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;为了减少热量的损失,大烧杯杯口与小烧杯杯口相平,图示装置中小烧杯口未用硬纸板盖住(或大烧杯内碎纸条塞少了,未将小烧杯垫的足够高),
故答案为:环形玻璃搅拌棒;小烧杯口未用硬纸板盖住(或大烧杯内碎纸条塞少了,未将小烧杯垫的足够高);
(2)氢氧化钠溶液和盐酸溶液的总体积为100mL,则小烧杯的规格应该为100mL,
故答案为:②;
(3)50mL0.50mol/L氢氧化钠与50mL0.55mol/L盐酸溶液进行中和反应,生成水的物质的量为:0.05L×0.50mol/L=0.025mol,溶液的质量为:100mL×1g/cm3=100g,温度变化的值为△T=(t2-t1)℃,则生成0.025mol水放出的热量为:Q=m•c•△T=100g×4.18J/(g•℃)×(t2-t1)℃=418(t2-t1)J,
所以实验测得的中和热△H=-$\frac{0.418({t}_{2}-{t}_{1})kJ}{0.025mol}$=-$\frac{0.418({t}_{2}{-t}_{1})}{0.025}$kJ/mol,
故答案为:-$\frac{0.418({t}_{2}{-t}_{1})}{0.025}$kJ/mol.
点评 本题考查了中和热的测定,题目难度中等,注意理解中和热的概念及测定反应热的方法,明确中和热的计算方法,试题培养了学生的化学计算和化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,它可由冰醋酸与过氧化氢在一定条件下制得;它可以迅速杀灭多种微生物,包括多种病毒(如:SARS病毒)、细菌、真菌及芽孢.有关过氧乙酸的叙述正确的是( )
| A. | 过氧乙酸不能使品红褪色 | |
| B. | 过氧乙酸可与苯酚混合使用 | |
| C. | 过氧乙酸分子中只含有极性键 | |
| D. | 过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体 |
10.已知A、B、C、D、E是短周期中原子序数依次增大的五种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的两倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 工业上常用电解法制备元素C、D、E的单质 | |
| B. | 元素A、B组成的化合物常温下一定呈气态 | |
| C. | 化合物AE与CE含有相同类型的化学键 | |
| D. | 元素C、D的最高价氧化物对应的水化物之间肯定不能发生反应 |
20.一定条件下,甲组内任意一种物质和乙组内任意一种物质都能发生反应的是
( )
| 甲 | 乙 | |
| A | H2、O2 | N2、CuO |
| B | HCl、NaOH | Fe、Al |
| C | SiO2、浓H2SO4 | NaOH、C |
| D | CO2、H2O | Na2O2、NaCl |
| A. | A | B. | B | C. | C | D. | D |
7.8.34g FeSO4•7H2O(分子量:278)样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,下列说法正确的是( )

| A. | 温度为78℃时固体物质M的化学式为FeSO4•5H2O | |
| B. | 取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe3O4 | |
| C. | 在隔绝空气条件下,N得到P的化学方程式为FeSO4•H2O $\frac{\underline{\;高温\;}}{\;}$FeSO4+H2O | |
| D. | 温度为l59℃时固体N的化学式为FeSO4•2H2O |
4.NA 表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 1mol 12C原子的质量是12g,1个12C原子的质量是$\frac{12}{{N}_{A}}$g | |
| B. | 在常温常压下,11.2LN2含有分子数为0.5NA | |
| C. | 18g水所含有的氢原子数目为2NA,氧原子数目为NA | |
| D. | 1L 0.1mol•L-1K2SO4溶液中,K+ 和SO42-的离子总数是0.3NA |