题目内容
7.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c1 | 0.2 | pH=7 |
| 丙 | 0.1 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱若a=7,HA为强酸;若a>7,HA为弱酸.
(2)不考虑其它组的实验结果,单从乙组情况分析,c1是否一定等于0.2mol/L否(填“是”或“否”).混合溶液中离子浓度c(A-)与c(Na+)的大小关系是C.
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是弱酸(填“强”或“弱”).该混合溶液中c(A-)+c(HA)=c(Na+)或0.05mol/L.
分析 (1)酸碱的物质的量相等,如为强酸,反应后溶液呈中性,如为弱酸,反应后溶液呈酸性;
(2)从HA的强弱以及溶液电中性的角度分析;
(3)HA为一元酸,反应生成NaA,溶液显示碱性,则HA为弱酸;根据物料守恒解答.
解答 解:(1)一元酸HA和NaOH溶液等体积混合,两种溶液的物质的量浓度都为0.2mol/L,则酸碱的物质的量相等,若a=7,说明反应后溶液呈中性,则HA是强酸,如a>7,反应后呈碱性,则HA是弱酸,
故答案为:若a=7,HA为强酸;若a>7,HA为弱酸;
(2)反应后溶液呈中性,如HA为强酸,则c=0.2,如HA为弱酸,则c>0.2,仅从乙组情况分析,c不一定等于0.2,
由于反应后溶液呈中性,则有c(OH-)=c(H+),根据溶液呈中性,则有c(Na+)+c(H+)=c(A-)+c(OH-),所以c(A-)=c(Na+),
故答案为:否;C;
(3)根据丙中数据可知,浓度相同的HA与氢氧化钠溶液反应恰好生成NaA,溶液的pH=9,溶液呈碱性,则生成的NaA为强碱弱酸盐,说明HA为弱酸;根据溶液中的物料守恒可得:c(A-)+c(HA)=c(Na+)=0.05 mol/L,
故答案为:弱酸;c(Na+)或0.05 mol/L.
点评 本题考查酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确弱电解质的电离和盐类水解原理为解答关键,注意掌握溶液酸碱性与溶液pH的关系,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
17.1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才.现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g)═2NH3(g)△H<0.当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示.

回答下列问题:
(1)已知:①NH3(l)═NH3(g)②N2(g)+3H2(g)═2NH3(l)△H2;则反应N2(g)+3H2(g)═2NH3(g)的△H=2△H1+△H2(用含△H1、△H2的代数式表示).
(2)合成氨的平衡常数表达式为$\frac{{c}^{3}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$,平衡时,M点NH3的体积分数为10%,则N2的转化率为18%(保留两位有效数字).
(3)X轴上a点的数值比b点小(填“大”或“小”).图中,Y轴表示温度(填“温度”或“压强”),判断的理由是随Y值增大,φ(NH3)减小,平衡N2(g)+3H2(g)?2NH3(g)△H<0向逆反应方向移动,故Y为温度.
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如表所示:
下列判断正确的是AB.
A.放出热量:Ql<Q2<△Hl B.N2的转化率:Ⅰ>ⅢC.平衡常数:Ⅱ>ⅠD.达平衡时氨气的体积分数:Ⅰ>Ⅱ
(5)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)>c(S042-)(填“>”、“<”或“=”).
(6)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y203)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-.写出负极的电极反应式2NH3+3O2--6e-=N2+3H2O.

回答下列问题:
(1)已知:①NH3(l)═NH3(g)②N2(g)+3H2(g)═2NH3(l)△H2;则反应N2(g)+3H2(g)═2NH3(g)的△H=2△H1+△H2(用含△H1、△H2的代数式表示).
(2)合成氨的平衡常数表达式为$\frac{{c}^{3}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$,平衡时,M点NH3的体积分数为10%,则N2的转化率为18%(保留两位有效数字).
(3)X轴上a点的数值比b点小(填“大”或“小”).图中,Y轴表示温度(填“温度”或“压强”),判断的理由是随Y值增大,φ(NH3)减小,平衡N2(g)+3H2(g)?2NH3(g)△H<0向逆反应方向移动,故Y为温度.
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如表所示:
| 容器编号 | 实验条件 | 平衡时反应中的能量变化 |
| Ⅰ | 恒温恒容 | 放热Q1kJ |
| Ⅱ | 恒温恒压 | 放热Q2kJ |
| Ⅲ | 恒容绝热 | 放热Q3kJ |
A.放出热量:Ql<Q2<△Hl B.N2的转化率:Ⅰ>ⅢC.平衡常数:Ⅱ>ⅠD.达平衡时氨气的体积分数:Ⅰ>Ⅱ
(5)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)>c(S042-)(填“>”、“<”或“=”).
(6)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y203)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-.写出负极的电极反应式2NH3+3O2--6e-=N2+3H2O.
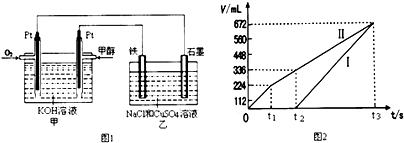
18. 按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )
按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )
 按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )
按如图所示装置连接,X、Y均为惰性电极.常温下,当Zn极质量减少3.25g时,X极生成气体840mL(标准状况),若此时烧杯中溶液的体积为500mL,则此时烧杯中溶液的pH(不考虑生成气体溶于水及与溶液的反应)( )| A. | 11 | B. | 12 | C. | 13 | D. | 14 |
15.氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )
| A. | AlON和石英的化学键类型相同 | |
| B. | AlON和石英晶体类型相同 | |
| C. | AlON中N元素的化合价为-1 | |
| D. | 电解熔融AlON或电解熔融Al2O3都能得到Al |
2.化学与人类生产、生活密切相关,下列说法正确的是( )
| A. | 铁的冶炼过程是通过置换反应得到单质铁 | |
| B. | 太阳能电池可采用硅材料制作,其应用有利于环保、节能 | |
| C. | 化学家采用玛瑙研钵磨擦固体反应物进行溶剂合成,玛瑙的主要成分是硅酸盐 | |
| D. | 包装食品里常有硅胶、生石灰、还原铁粉三类小包,其作用相同 |
17.下列事故处理或操作不正确的是( )
| A. | 不慎碰倒酒精灯,洒出的酒精在桌上燃烧时,应立即用湿抹布扑盖 | |
| B. | 不慎将浓硫酸溅到皮肤上,应先用布抹去,再用大量水冲洗,最后涂上碳酸氢钠溶液 | |
| C. | 制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 | |
| D. | 实验室制取氧气完毕后,应停止加热,再取出集气瓶,最后取出导气管 |
 科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.
科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.