题目内容
下列关于化学电源的说法不正确的是( )
| A、我们可以根据硫酸密度的大小来判断铅蓄电池是否需要充电 |
| B、燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为热能,然后再转化为电能的化学电源 |
| C、普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,就不能再使用了 |
| D、由Ag2O和Zn形成的碱性银锌纽扣电池,发生电化学反应时,Zn作为负极 |
考点:常见化学电源的种类及其工作原理
专题:
分析:A.铅蓄电池电池反应式为Pb+PbO2+4H++2SO42-
2PbSO4+2H2O,放电时硫酸参加反应生成水,导致溶质质量减小、溶液质量增大,充电时有硫酸生成,溶质的质量增大、溶剂的质量减小;
B.燃料电池是将化学能转化为电能;
C.普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,不能被复原;
D.原电池中,易失电子的金属作负极.
| 放电 |
| 充电 |
B.燃料电池是将化学能转化为电能;
C.普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,不能被复原;
D.原电池中,易失电子的金属作负极.
解答:
解:A.铅蓄电池电池反应式为Pb+PbO2+4H++2SO42-
2PbSO4+2H2O,放电时硫酸参加反应生成水,导致溶质质量减小、溶液质量增大,密度减小,充电时,生成硫酸,溶质的质量增大、溶剂的质量减小,溶液密度增大,则可以根据硫酸密度的大小来判断铅蓄电池是否需要充电,故A正确;
B.燃料电池是将化学能转化为电能,不需要将化学能转化为热能,故B错误;
C.普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,不能被复原,所以就不能再使用了,故C正确;
D.原电池中,易失电子的金属作负极,该原电池中,Zn易失电子而作负极,故D正确;
故选B.
| 放电 |
| 充电 |
B.燃料电池是将化学能转化为电能,不需要将化学能转化为热能,故B错误;
C.普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,不能被复原,所以就不能再使用了,故C正确;
D.原电池中,易失电子的金属作负极,该原电池中,Zn易失电子而作负极,故D正确;
故选B.
点评:本题考查原电池和电解池原理,侧重考查分析问题、解答问题能力,知道原电池中能量转化、正负极的判断、正负极上电极反应式,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
下列溶液在空气中加热、蒸干、灼烧后,所得固体为原溶液中的溶质的是( )
| A、(NH4)2SO3 |
| B、KMnO4 |
| C、AlCl3 |
| D、Na2CO3 |
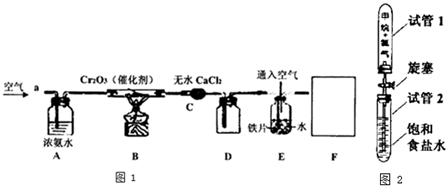
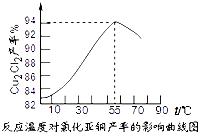 氯化亚铜(Cu2Cl2)是一种重要的化工产品,常用作有机合成催化剂.已知:
氯化亚铜(Cu2Cl2)是一种重要的化工产品,常用作有机合成催化剂.已知: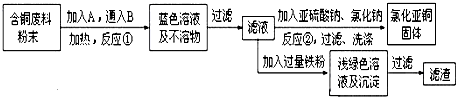







 针对化学反应中的能量变化解决下列问题.
针对化学反应中的能量变化解决下列问题.