题目内容
14.下列说法错误的是( )| A. | 11H、21H、31H、H+和H2是氢元素的五种不同粒子 | |
| B. | 白磷和红磷的相互转化属于物理变化 | |
| C. | 11H和21H是不同的核素 | |
| D. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
分析 A.氢元素的粒子可以指的是原子、分子和离子,其中同位素是同种元素的不同原子属于不同粒子;
B.同素异形体的结构不同,转化属于化学变化;
C.核素指的是一定质子数和一定中子数原子;
D.同位素是质子数相同、中子数不同的原子,质子数相同原子的最外层电子数相同,最外层电子数决定元素的化学性质;
解答 解:A.11H、12H、13H是氢元素的三种不同粒子,H+表示氢离子,H2表示氢气分子,是氢元素的五种不同粒子,故A正确;
B.白磷和红磷是同种元素形成的不同种单质,互为同素异形体,结构不同,原子最外层电子数相同,物理性质不同,化学性质相似,相互转化为化学变化,故B错误;
C.1H和2H质子数相同,质量数不同,属于不同的核素.故C正确;
D.同位素是质子数相同、中子数不同的原子,质子数相同原子的最外层电子数相同,最外层电子数决定元素的化学性质,12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同,故D正确;
故选B.
点评 本题主要考查的是同位素、同素异形体、核素的概念,难度不大,注意区别这两个概念实质,掌握基础是解题关键.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
4.下列各组物质中,化学键类型完全相同的是( )
| A. | SiO2和H2O | B. | SO2和Na2O2 | C. | NaCl和HCl | D. | AlCl3和KCl |
5.反应4A(g)+5B(g)═4C(g)+4D(g)在0.5L密闭容器中进行,30s后A减少了0.90mol,则此反应的速率可表示为( )
| A. | v(A)=0.030 mol/(L•s) | B. | v(B)=0.075 mol/(L•s) | ||
| C. | v(C)=0.030 mol/(L•s) | D. | v(D)=0.030 mol/(L•s) |
2.下列措施肯定能使反应速率增大的是( )
| A. | 增大反应物的量 | B. | 增大压强 | C. | 适当升高温度 | D. | 使用催化剂 |
9.下列四种有机化合物均含有多个官能团,其结构简式如下所示,下列有关说法中正确的是( )
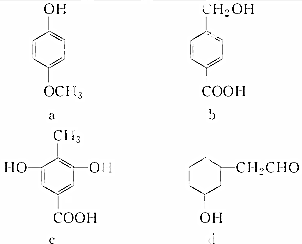

| A. | a属于酚类,可与NaHCO3溶液反应产生CO2 | |
| B. | b属于酚类,1 molb最多能与3 molH2发生加成反应 | |
| C. | 1 mol c最多能与3 mol Br2发生反应 | |
| D. | d属于醇类,可以发生消去反应 |
3.属于天然高分子化合物的组合是( )
| A. | 聚乙烯、淀粉 | B. | 油脂、蛋白质 | C. | 酚醛树脂、纤维素 | D. | 纤维素、淀粉 |
 在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是(“氧化”或“还原”)氧化反应,银电极上的电极反应式为Cu2++2e-═Cu.
在银锌原电池中,以硫酸铜为电解质溶液,锌为负极,电极上发生的是(“氧化”或“还原”)氧化反应,银电极上的电极反应式为Cu2++2e-═Cu.
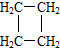 可简写成
可简写成 )
)
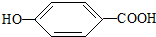 ),其反应方程式为:
),其反应方程式为: 、
、 .
.