题目内容
4.下列各组物质中,化学键类型完全相同的是( )| A. | SiO2和H2O | B. | SO2和Na2O2 | C. | NaCl和HCl | D. | AlCl3和KCl |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,以此来解答.
解答 解:A.均只含共价键,故A选;
B.SO2含共价键,Na2O2含离子键和共价键,故B不选;
C.NaCl含离子键,HCl含共价键,故C不选;
D.AlCl3含共价键,KCl含离子键,故D不选;
故选A.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中化学键的判断,选项D为易错点,题目难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
11.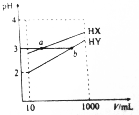 常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
 常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )
常温下,10mL浓度均为0.1mol/L的HX和HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如图所示.则下列说法正确的是( )| A. | HX的电离常数K(HX)大于HY的电离常数K(HY) | |
| B. | a点水的电离程度大于b点水的电离程度 | |
| C. | a、b两点对应的两种酸等体积混合后溶液的pH大于混合前溶液的pH | |
| D. | 浓度均为0.1mol/L的NaX和NaY组成的混合溶液中c(Na+)>c(Y-)>c(X-)>c(OH-)>c(H+) |
15.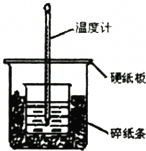 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒,仍存在的缺陷是大小烧杯间未用碎纸条填满,大小烧杯杯口未平.
(2)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1>△H(填“<”、“>”或“=”).
(3)写出该反应的中和热的热化学方程式(中和热为57.3kJ/mol):NaOH(aq)+1/2H2SO4(aq)=l/2Na2SO4(aq)+H2O(aq)AH=-57.3kJ•mol-1.
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,装置已做改进.实验数据如表.
又已知0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都近似为1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-43.5kJ.mol-1(取小数点后一位).
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把H2SO4溶液倒入盛有NaOH溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后未清洗直接测定H2SO4溶液的温度
e.实验当天气温较高.
 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒,仍存在的缺陷是大小烧杯间未用碎纸条填满,大小烧杯杯口未平.
(2)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1>△H(填“<”、“>”或“=”).
(3)写出该反应的中和热的热化学方程式(中和热为57.3kJ/mol):NaOH(aq)+1/2H2SO4(aq)=l/2Na2SO4(aq)+H2O(aq)AH=-57.3kJ•mol-1.
(4)取50mL NaOH溶液和30mL硫酸溶液进行实验,装置已做改进.实验数据如表.
| 起始温度/℃ | 终止温度/℃ | 温度差/℃ | |||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.35 | 27.6 | 3.25 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把H2SO4溶液倒入盛有NaOH溶液的小烧杯中
d.用温度计测定NaOH溶液起始温度后未清洗直接测定H2SO4溶液的温度
e.实验当天气温较高.
19. 下面是18×7的格子,按要求作答
下面是18×7的格子,按要求作答
(1)用封闭的实线绘出元素周期表的轮廓,注意:不得使用铅笔作图.
(2)C元素的一种中子数为10的同位素的原子符号为818O,C2-的离子结构示意图为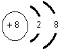 ,C、D、E、F的简单离子半径由小到大顺序是Al3+<Mg2+<F-<O2-.(填写离子符号 )
,C、D、E、F的简单离子半径由小到大顺序是Al3+<Mg2+<F-<O2-.(填写离子符号 )
(3)A、G、C中的2种或3种元素能形成18个电子的分子N2H4、H2O2(填化学式),其中A、G也能形成GA5的离子化合物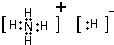 (填电子式).
(填电子式).
(4)请分别用1个离子方程式说明B和F的金属性强弱:Al3++3OH-=Al(OH)3↓或Al(OH)3+OH-=AlO2-+2H2O,C和D的非金属性强弱2F2+2H2O=4HF+O2.
(5)Fe位于周期表第四周期VIII族,请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱.写出总反应式:2 Fe3++Cu=2Fe2++Cu2+负极电极反应式:Cu-2e-=Cu2+,并在方框内画出实验装置图,并标注电极材料和电解质溶液.
 下面是18×7的格子,按要求作答
下面是18×7的格子,按要求作答| A | He | ||||||||||||||||
| G | C | D | |||||||||||||||
| B | E | F | I | H | |||||||||||||
| Fe | Cu | ||||||||||||||||
(2)C元素的一种中子数为10的同位素的原子符号为818O,C2-的离子结构示意图为
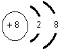 ,C、D、E、F的简单离子半径由小到大顺序是Al3+<Mg2+<F-<O2-.(填写离子符号 )
,C、D、E、F的简单离子半径由小到大顺序是Al3+<Mg2+<F-<O2-.(填写离子符号 )(3)A、G、C中的2种或3种元素能形成18个电子的分子N2H4、H2O2(填化学式),其中A、G也能形成GA5的离子化合物
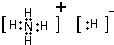 (填电子式).
(填电子式).(4)请分别用1个离子方程式说明B和F的金属性强弱:Al3++3OH-=Al(OH)3↓或Al(OH)3+OH-=AlO2-+2H2O,C和D的非金属性强弱2F2+2H2O=4HF+O2.
(5)Fe位于周期表第四周期VIII族,请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱.写出总反应式:2 Fe3++Cu=2Fe2++Cu2+负极电极反应式:Cu-2e-=Cu2+,并在方框内画出实验装置图,并标注电极材料和电解质溶液.
9.我国古代做衣服的主要原料是麻和丝.下列有关说法中不正确的是( )
| A. | 麻的主要成分表示为(C6H1206) | |
| B. | 丝的主要成分是蛋白质 | |
| C. | 麻和丝生要成分均属于高分子化合物 | |
| D. | 麻和丝可以通过灼烧进行区分 |
14.下列说法错误的是( )
| A. | 11H、21H、31H、H+和H2是氢元素的五种不同粒子 | |
| B. | 白磷和红磷的相互转化属于物理变化 | |
| C. | 11H和21H是不同的核素 | |
| D. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
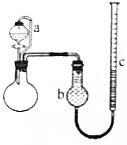 某研究性学习小组为了测定镀锌薄铁板(假设只含Fe和Zn)中锌的质量分数ω(Zn),用如图所示装置(夹持装置略去)进行实验,通过测定产生H2的体积计算ω(Zn).已知:①锌易溶于强碱溶液,发生反应为Zn+2NaOH═Na2ZnO2+H2↑.②所用的镀锌薄铁板均为m1g.回答下列问题:
某研究性学习小组为了测定镀锌薄铁板(假设只含Fe和Zn)中锌的质量分数ω(Zn),用如图所示装置(夹持装置略去)进行实验,通过测定产生H2的体积计算ω(Zn).已知:①锌易溶于强碱溶液,发生反应为Zn+2NaOH═Na2ZnO2+H2↑.②所用的镀锌薄铁板均为m1g.回答下列问题: