题目内容
18.下列说法错误的是( )| A. | 在共价化合物中一定含有共价键 | |
| B. | 含有离子键的化合物一定就是离子化合物 | |
| C. | 双原子单质分子中的共价键一定是非极性键 | |
| D. | 原子最外层电子数大于4的元素一定是非金属元素 |
分析 A、只含有共价键的化合物是共价化合物;
B、离子化合物一定含有离子键;
C、相同元素形成的共价键是非极性键;
D、非金属元素的最外层电子数一般大于4;
解答 解:A、只含有共价键的化合物是共价化合物,所以在共价化合物中一定含有共价键,故A正确;
B、离子化合物一定含有离子键,所以含有离子键的化合物是离子化合物,故B正确;
C、相同元素形成的共价键是非极性键,所以双原子单质分子中的共价键一定是非极性键,故C正确;
D、非金属元素的最外层电子数一般大于4,在反应中易得到电子,则原子最外层电子数大于4的元素一定是非金属元素,但某些金属元素的最外层电子数大于4,如锑和铋等,故D错误;
故选D.
点评 本题考查了化学键和化合物的关系,难度不大,注意只含有共价键的化合物是共价化合物.

练习册系列答案
相关题目
8.下列过程中,共价键被破坏的是( )
| A. | 碘升华 | B. | 溴蒸气被木炭吸附 | ||
| C. | 加热使氯化铵分解 | D. | 氯化氢气体溶于水 |
6.下列陈述 I、陈述 II均正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2能使溴水褪色 | SO2具有还原性 |
| B | NH3能使酚酞溶液变红 | NH3可用于设计喷泉 |
| C | SiO2能与氢氟酸、碱反应 | SiO2是两性氧化物 |
| D | 晶体Si熔点高硬度大 | 晶体Si可用作半导体材料 |
| A. | A | B. | B | C. | C | D. | D |
3.若某原子的摩尔质量是M g/mol,则一个该原子的真实质量是( )
| A. | M g | B. | $\frac{1}{M}$g | C. | $\frac{6.02×1{0}^{23}}{M}$g | D. | $\frac{M}{{N}_{A}}$g |
7.下列说法正确的是( )
| A. | 从石油中获得乙烯,已成为目前工业上生产乙烯的主要途径 | |
| B. | 催化剂一般在金属与非金属的分界处寻找 | |
| C. | 硅是一种良好的导热、导电材料 | |
| D. | 氢的同位素${\;}_{1}^{1}$H可用于制造氢弹 |
8.将下列溶液置于敞口容器中,溶液质量会出现增重的是( )
| A. | 浓氨水 | B. | 浓盐酸 | C. | 浓H2SO4 | D. | 浓硝酸 |
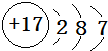
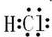 ;
;