题目内容
8.下列过程中,共价键被破坏的是( )| A. | 碘升华 | B. | 溴蒸气被木炭吸附 | ||
| C. | 加热使氯化铵分解 | D. | 氯化氢气体溶于水 |
分析 一般非金属元素之间形成共价键,由共价键形成的物质在溶于水、化学变化中共价键被破坏,以此来解答.
解答 解:A.碘升华克服的是分子间作用力,共价键没有破坏,故A错误;
B.木炭吸附是物理变化,故B错误;
C.加热使氯化铵分解生成氨气和氯化氢,存在共价键破坏,故C正确;
D.HCl气体溶于水,发生电离,共价键被破坏,故D正确.
故选CD.
点评 本题考查化学键知识,题目难度不大,注意共价键、离子键以及分子间作用力的区别.

练习册系列答案
相关题目
18.工业上电解氧化铝要求其纯度不得低于98.2%,而天然铝土矿的氧化铝含量为50%~70%,杂质主要为SiO2、Fe2O3、CaO、MgO、Na2O等.工业生产铝锭的工艺流程示意图如下:
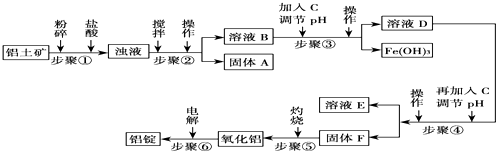
部分氢氧化物沉淀的pH如下表
请回答下列问题:
(1)加入盐酸时,氧化铝发生反应的离子方程式为Al2O3+6H+═2Al3++3H2O.
(2)实验室进行步骤②的操作名称为过滤,其使用到的玻璃仪器是漏斗、烧杯、玻璃棒.
(3)固体A的化学式为SiO2,物质C的化学式为NaOH[或Ca(OH)2];溶液中的Na+、Ca2+、Mg2+是在步骤④(填序号)中分离出去的.
(4)步骤③调节pH的数值范围为4.1≤pH<4.3,步骤④调节pH的数值范围为5.2≤pH<10.4.

部分氢氧化物沉淀的pH如下表
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH2 |
| 开始沉淀pH (离子初始浓度0.01mol/L) | 4.3 | 2.3 | 10.4 |
| 完全沉淀pH (离子浓度<10-5 mol/L) | 5.2 | 4.1 | 12.4 |
(1)加入盐酸时,氧化铝发生反应的离子方程式为Al2O3+6H+═2Al3++3H2O.
(2)实验室进行步骤②的操作名称为过滤,其使用到的玻璃仪器是漏斗、烧杯、玻璃棒.
(3)固体A的化学式为SiO2,物质C的化学式为NaOH[或Ca(OH)2];溶液中的Na+、Ca2+、Mg2+是在步骤④(填序号)中分离出去的.
(4)步骤③调节pH的数值范围为4.1≤pH<4.3,步骤④调节pH的数值范围为5.2≤pH<10.4.
19.对于放热反应H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,下列说法中,正确的是( )
| A. | 生成物所具有的总能量高于反应物所具有的总能量 | |
| B. | 反应物所具有的总能量高于生成物所具有的总能量 | |
| C. | 断开1 mol H-H键和1 mol Cl-Cl键所吸收的总能量大于形成2mol H-Cl键所放出的能量 | |
| D. | 该反应中,化学能只转变为热能 |
13.2016年1月1日起修订厉的《中华人民共和国大气污染防治法》正式施行,这将对我国的大气污染防治产生重要影响.下列有关说法正确的是( )
| A. | 绿色食品就是不含任何化学物质的食品 | |
| B. | 燃煤时添加生石灰以减少SO2的排放 | |
| C. | PM2.5是指环境空气中直径小于或等于2.5微米的颗粒物 | |
| D. | pH在5.6~7.0之间的降水通常称为酸雨 |
20.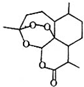 屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
 屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )
屠呦呦1971年发现、分离、提纯并用于治疟新药“青蒿素”,拯救了数千万人的生命.青蒿素分子结构如图.下列说法错误的是( )| A. | 青蒿素的分子式为C15H22O5 | B. | 青蒿素是芳香族化合物 | ||
| C. | 青蒿素可以发生水解反应 | D. | 青蒿素不能使酸性KMnO4溶液褪色 |
18.下列说法错误的是( )
| A. | 在共价化合物中一定含有共价键 | |
| B. | 含有离子键的化合物一定就是离子化合物 | |
| C. | 双原子单质分子中的共价键一定是非极性键 | |
| D. | 原子最外层电子数大于4的元素一定是非金属元素 |
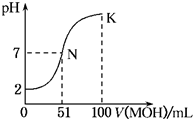 常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题: