题目内容
16.下列关于化学反应速率的说法正确的是( )| A. | 1L0.1mol/L盐酸和1L0.1mol/L硫酸分别与1L2mol/LNaOH溶液反应的反应速率相同 | |
| B. | 化学反应速率为0.8mol/(L•s),其含义是时间为1s时,某物质的浓度是0.8mol/L | |
| C. | 等体积的0.1mol/L盐酸和0.1mol/L硝酸与形状和大小相同的大理石反应的速率相同 | |
| D. | 对于任何化学反应来说,反应速率越大,反应现象就越明显 |
分析 A.同浓度的盐酸和硫酸的氢离子浓度不同;
B.化学反应速率为0.8mol/(L•s),含义为单位时间内浓度变化0.8mol/L;
C.浓度相同,固体表面积相同,则反应速率相同;
D.反应速率大小与反应现象没有必然的联系.
解答 解:A.同浓度的盐酸和硫酸的氢离子浓度不同,则与等浓度的氢氧化钠反应的速率不同,故A错误;
B.化学反应速率为“0.8mol/(L•s)”表示的意思是:时间段为1s时,某物质的浓度增加或减少0.8mol/L,故B错误;
C.等体积的0.1mol/L盐酸和0.1mol/L硝酸浓度相同,大理石固体表面积相同,则反应速率相同,故C正确;
D.反应速率快的现象不一定明显,如NaOH与HCl的反应,反应速率慢的现象可能明显,如铁生锈,故D错误.
故选C.
点评 本题考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力的考查,注意外界条件对活化分子的影响,难度不大.

练习册系列答案
相关题目
6.雾霾天气严重影响人们的生活,其中氮氧化物和硫氧化物都是形成雾霾天气的重要因素.下列方法可处理氮氧化物和硫氧化物.
(1)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,在一定条件下,发生反应:C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ/mol.
在T1℃时,反应进行到不同时间测得各物质的浓度如表.
①0~10min内,NO的平均反应速率v(NO)=0.042mol/(L•min),T1℃时,该反应的平衡常数K=$\frac{9}{16}$.
②若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:1:1,则Q<(填“>”、“=”或“<”)0.
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图甲所示.

①由图甲可知,SCR技术中的氧化剂为NO、NO2.已知c(NO2):c(NO)=1:1时脱氮效果最佳,若生成1mol N2时反应放出的热量为Q kJ.此时对应的脱氮反应的热化学方程式为2NH3(g)+NO(g)+NO2(g)═2N2(g)+3H2O(g)△H=-2QkJ/mol.
②图乙是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业选取的最佳催化剂及相应的温度分别为Mn、200℃.
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,若所得溶液呈中性,则该溶液中c(Na+)=2c(SO32-)+c(HSO3-)(用含硫微粒浓度的代数式表示).
(4)某研究小组用NaOH溶液吸收二氧化硫后,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图丙所示,电极材料为石墨.
①a表示阳(填“阴”或“阳”)膜.A-E分别代表原料或产品.
其中C为稀硫酸,则A为NaOH溶液(填写化学式)
②阳极电极反应式为SO32--2e-+H2O=SO42-+2H+.
(1)用活性炭还原法可以处理氮氧化物.某研究小组向某密闭容器中加入一定量的活性炭和NO,在一定条件下,发生反应:C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ/mol.
在T1℃时,反应进行到不同时间测得各物质的浓度如表.
浓度/mol/L 时间/min | 0 | 10 | 20 | 30 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 |
| N2 | 0 | 0.21 | 0.30 | 0.30 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 |
②若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:1:1,则Q<(填“>”、“=”或“<”)0.
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图甲所示.

①由图甲可知,SCR技术中的氧化剂为NO、NO2.已知c(NO2):c(NO)=1:1时脱氮效果最佳,若生成1mol N2时反应放出的热量为Q kJ.此时对应的脱氮反应的热化学方程式为2NH3(g)+NO(g)+NO2(g)═2N2(g)+3H2O(g)△H=-2QkJ/mol.
②图乙是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业选取的最佳催化剂及相应的温度分别为Mn、200℃.
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,若所得溶液呈中性,则该溶液中c(Na+)=2c(SO32-)+c(HSO3-)(用含硫微粒浓度的代数式表示).
(4)某研究小组用NaOH溶液吸收二氧化硫后,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图丙所示,电极材料为石墨.
①a表示阳(填“阴”或“阳”)膜.A-E分别代表原料或产品.
其中C为稀硫酸,则A为NaOH溶液(填写化学式)
②阳极电极反应式为SO32--2e-+H2O=SO42-+2H+.
7.将22.4g铜锌合金均分为两份,向一份中加400mL一定浓度的稀硝酸,二者恰好完全反应,生成标准状况下的NO气体4.48L,若将另一份充分加热至质量恒重时,则生成的固体质量为( )
| A. | 32.0g | B. | 16.0 | C. | 18.0 | D. | 36.0 |
4.下列说法正确的是( )
| A. | 向鸡蛋清的溶液中加入浓的硫酸铵溶液,蛋白质的性质发生改变并凝聚 | |
| B. | 将牛油和烧碱溶液混合加热,充分反应后加入热的饱和食盐水,下层析出肥皂 | |
| C. | 油脂为髙分子化合物,分子结构中都含有酯基 | |
| D. | 纤维素、麦芽糖在一定条件下均可转化为葡萄糖 |
11.下列说法正确的是( )
| A. | 氯气和液氯是两种不同的物质 | |
| B. | NH3是电解质,所以氨水能导电 | |
| C. | 氨不能用浓硫酸干燥,但可以用无水CaCl2干燥 | |
| D. | 新制的氯水呈酸性,向其中滴加几滴紫色石蕊试液并振荡,溶液先变红后褪色 |
1.下列物质分类不正确的是( )
| A. | 化合物:干冰、冰水共存物、烧碱、小苏打 | |
| B. | 同素异形体:活性炭、C60、石墨烯、金刚石 | |
| C. | 非电解质:氨气、二氧化硫、铜、乙醇 | |
| D. | 混合物:铝热剂、纯净矿泉水、分析纯盐酸、漂白粉 |
20.只含一个三键的炔烃A加氢后的产物的结构简式为 ,炔烃A可能的结构简式有( )
,炔烃A可能的结构简式有( )
 ,炔烃A可能的结构简式有( )
,炔烃A可能的结构简式有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
1.2007年10月,一台湾女孩因食用河虾后服用大剂量的维生素C而中毒.菜谱中记载:河虾不宜与西红柿同食.主要原因是河虾中含有+5价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的+3价砷.下列说法正确的是( )
| A. | 在该反应中维生素C作催化剂 | |
| B. | 因为河虾中含有砷元素,所以不能食用 | |
| C. | 砒霜是砷的氧化物,由上述可推知砒霜中含有的砷是+3价 | |
| D. | 上述反应中维生素C作氧化剂 |
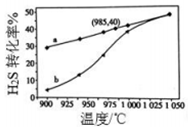 废气中的H2S通过高温热分解可制取氢气:2H2S(g)?2H2(g)+S2(g).在3L密闭容器中,控制不同温度进行H2S分解实验.
废气中的H2S通过高温热分解可制取氢气:2H2S(g)?2H2(g)+S2(g).在3L密闭容器中,控制不同温度进行H2S分解实验.