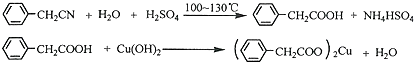
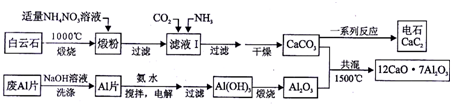
��Ŀ����
14����ҵ�����÷�̼�����Ҫ�ɷ�CeCO3F����ȡCeCl3��һ�ֹ����������£�
��ش��������⣺
��1��CeCO3F�У�CeԪ�صĻ��ϼ�Ϊ+3��
��2�������������ϡ�����H2O2�滻HCl������ɻ�����Ⱦ��д��ϡ���ᡢH2O2��CeO2��Ӧ�����ӷ���ʽ��H2O2+2CeO2+6H+=2Ce3++4H2O+O2����
��3����Ce��BF4��3�м���KCl��Һ��Ŀ���DZ�����������Ce��BF4��3��������ʽ��ʧ���ȥBF4-�����CeCl3�IJ��ʣ�
��4����Һ�е�C��Ce3+������1��10-5mol•l-1������ΪCe3+������ȫ����ʱ��Һ��PHΪ9��
����֪KSP[Ce��OH��3]=1��10-20��
��5������CeCl3.6H2O��NH4Cl�Ĺ�������ɵõ���ˮCeCl3������NH4Cl��������NH4Cl�������ȷֽ����HCl������CeCl3ˮ�⣮
��6��ȷ��ȡ0.7500gCeCl3��Ʒ������ƿ�У������������������Һ��Ce3+����ΪCe4+��Ȼ����0.1000mol��l-1��NH4��2Fe��SO4��2����Һ�ζ����յ㣬����25.00ml����Һ������֪��Fe2+Ce4+=Ce3++Fe3+��
�ٸ���Ʒ��CeCl3����������Ϊ82.2%��
����ʹ�þ��õģ�NH4��2Fe��SO4��2����Һ���еζ�����ø�CeCl3��Ʒ����������ƫ���ƫ����ƫС������Ӱ�족��
���� ���÷�̼�����Ҫ�ɷ�CeCO3F����ȡCeCl3��һ�ֹ�������Ϊ��CeCO3F���յ�CeO2��CeF4���������������������˵ó���Ce��BF��4��CeCl3��Һ��Ce��BF��4���Ȼ�����Һ��Ӧ�õ�CeCl3��KBF��CeCl3��ǰ����Һ��CeCl3�ĺϲ��ټ��������ƣ���Ce��OH��3������Ce��OH��3���������ᷴӦ�ɵ�CeCl3•6H2O������CeCl3•6H2O��NH4Cl�Ĺ�������ɵõ���ˮCeCl3��
��1�����ݻ��ϼ۴�����Ϊ0�жϣ�
��2��������������H2O2�ܻ�ԭCeO2����Ce3+������Ԫ���غ�͵���غ���д���ӷ���ʽ��
��3����Ce��BF4��3�м���KCl��Һ����CeCl3��KBF����ֹ����Ce��BF4��3������
��4����Һ�е�C��Ce3+������1��10-5mol•L-1������ΪCe3+������ȫ������KSP[Ce��OH��3]=C��Ce3+��•C3��OH-�� �ɼ������Һ�����������ӵ�Ũ�ȣ�����ȷ��PHֵ��
��5��NH4Cl�������ȷֽ����HCl����������CeCl3ˮ�⣬�ݴ˴��⣻
��6����0.1000mol•l-1��NH4��2Fe��SO4��2����Һ���25.00ml�������������ӵ����ʵ���Ϊ2.5��10-3mol�����ݷ�ӦFe2++Ce4+�TCe3++Fe3+������CeԪ���غ��֪���ɼ����CeCl3������������ȷ����Ʒ��CeCl3������������
����ʹ�þ��õģ�NH4��2Fe��SO4��2����Һ���еζ��������������ӱ��������������������Ի����ı�Һ�����Ϊƫ�ݴ˷�����
��� �⣺���÷�̼�����Ҫ�ɷ�CeCO3F����ȡCeCl3��һ�ֹ�������Ϊ��CeCO3F���յ�CeO2��CeF4���������������������˵ó���Ce��BF��4��CeCl3��Һ��Ce��BF��4���Ȼ�����Һ��Ӧ�õ�CeCl3��KBF��CeCl3��ǰ����Һ��CeCl3�ĺϲ��ټ��������ƣ���Ce��OH��3������Ce��OH��3���������ᷴӦ�ɵ�CeCl3•6H2O������CeCl3•6H2O��NH4Cl�Ĺ�������ɵõ���ˮCeCl3��
��1�����ݻ��ϼ۴�����Ϊ0��֪��CeCO3F�У�CeԪ�صĻ��ϼ�Ϊ+3�ۣ�
�ʴ�Ϊ��+3��
��2��ϡ���ᡢH2O2��CeO2��Ӧ�����ӷ���ʽΪ��H2O2+2CeO2+6H+=2Ce3++4H2O+O2����
�ʴ�Ϊ��H2O2+2CeO2+6H+=2Ce3++4H2O+O2����
��3����Ce��BF4��3�м���KCl��Һ����CeCl3��KBF����������Ŀ���DZ�����������Ce��BF4��3��������ʽ��ʧ���ȥBF4-�����CeCl3�IJ��ʣ�
�ʴ�Ϊ��������������Ce��BF4��3��������ʽ��ʧ���ȥBF4-�����CeCl3�IJ��ʣ�
��4����Һ�е�C��Ce3+������1��10-5mol•L-1������ΪCe3+������ȫ������KSP[Ce��OH��3]=C��Ce3+��•C3��OH-��=1��10-20��֪��C��OH-��=$\root{3}{\frac{1��1{0}^{-20}}{1��1{0}^{-5}}}$mol•L-1=1��10-5mol•L-1����ʱ��Һ��PHΪ9��
�ʴ�Ϊ��9��
��5������NH4Cl�������ȷֽ����HCl������CeCl3ˮ�⣬���Լ���CeCl3•6H2O��NH4Cl�Ĺ�������ɵõ���ˮCeCl3��
�ʴ�Ϊ��NH4Cl�������ȷֽ����HCl������CeCl3ˮ�⣻
��6����0.1000mol•l-1��NH4��2Fe��SO4��2����Һ���25.00ml�������������ӵ����ʵ���Ϊ2.5��10-3mol�����ݷ�ӦFe2++Ce4+�TCe3++Fe3+������CeԪ���غ��֪��CeCl3������Ϊ2.5��10-3mol��246.5g/mol=0.6163g��������Ʒ��CeCl3����������Ϊ$\frac{0.6163g}{0.7500g}$��100%=82.2%��
�ʴ�Ϊ��82.2%��
����ʹ�þ��õģ�NH4��2Fe��SO4��2����Һ���еζ��������������ӱ��������������������Ի����ı�Һ�����Ϊƫ�����ø�CeCl3��Ʒ����������ƫ��
�ʴ�Ϊ��ƫ��
���� ��������ȡCeCl3��һ�ֹ�������Ϊ���壬�����˻��ϼۡ����ӷ�Ӧ�������ܽ�ƽ��ļ��㡢ʵ�������������ѧ�����֪ʶ�����ط������ƶϼ�ʵ���������ۺϿ��飬��Ŀ�Ѷ��еȣ�

 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�| A�� | ԭ��Һ��һ������SO42-��NH4+��Cl- | |
| B�� | ԭ��Һ��һ��������Br-��Fe2+��SO32- | |
| C�� | ԭ��Һ�п��ܴ���SO32-��K+ | |
| D�� | ԭ��Һ�еζ�����K+��c��K+����0.2mol•L-1 |
| A�� | �ռ�Cl2���ű���ʳ��ˮ�ķ��� | |
| B�� | �Ӵ�����ʹSO2��O2 ��һ��������ת��ΪSO3 | |
| C�� | ����Ũ��ˮ��NaOH��s��������ȡ���� | |
| D�� | ��ѹ������������N2��H2��Ӧ����NH3 |
���������繤ҵ����̼���Ƶķ�����·������N��Leblanc���������������£�
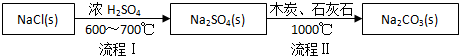
��1������I����һ������HCl�����̢�ķ�Ӧ�ֲ����У�a��Na2SO4+4C $\frac{\underline{\;1000��\;}}{\;}$Na2S+4CO����
b��Na2S��ʯ��ʯ�������ֽⷴӦ���ܷ�Ӧ����ʽ�ɱ�ʾΪNa2SO4+4C+CaCO3$\frac{\underline{\;1000��\;}}{\;}$Na2CO3+CaS+4CO����
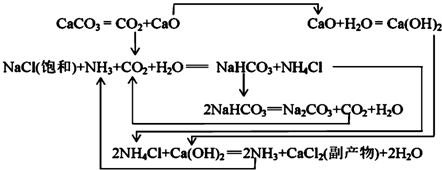
��1862�꣬����ʱ������ά��Ernest Solvay���ð������̼���ƣ���Ӧԭ�����£�
20��ʱһЩ������ˮ�е��ܽ��/g•��100gH2O��-1
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
��3������NaCl��ҺͨNH3��CO2������NaHCO3��ԭ���У���Ӧ��ϵ��NaHCO3�ܽ����С����Ӧ����ˮ��NaHCO3��Է����������
���ҹ�����ר�Һ�°��о��������Ƽ���䷴Ӧԭ���Ͱ�����ƣ������ư����Ƽ����ϣ������ԭ�������ʣ�
��4����������������NaHCO3�����õ���Һ�м���NaCl���岢ͨ��NH3����0��10�棨���¶ȷ�Χ��������NH4Cl�����ѧʽ��
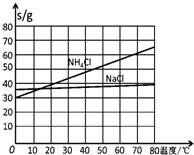
��֪��

�ٱ����ױ�������
�����������������ʹ���IJ����������������
| ���� | �۵�/�� | �е�/�� | �ܽ��� |
| �������� | 114.3 | 305 | ������ˮ����������ˮ |
| ���� | -6 | 184.4 | ����ˮ |
| ���� | 16.6 | 118 | ������ˮ |
����1����a�У�����9mL ��0.10mol��������15mL��0.27mol�������ἰ����п�ۣ�����ͼװ����װ������
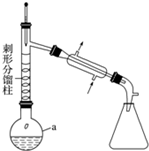
����2�������¶ȼƶ�����105�����ң�С����Ȼ�������Ӧ��ȫ��
����3�����Ƚ���Ӧ����ﵹ��ʢ��100mL ��ˮ���ձ��У���ȴ����ˡ�ϴ�ӣ��õ��ֲ�Ʒ��
����4��������3���ôֲ�Ʒ��һ���ᴿ�Ƶò�Ʒ����Ϊ10.8g��
��ش��������⣺
��1������a������ΪԲ����ƿ����ѡ����a����ѹ����B������ţ���
A�� 25mL B��50mL C��100mL D��250mL
��2��ʵ���м�������п�۵�Ŀ���Ƿ�ֹ������������ͬʱ���ŷ�ʯ�����ã�
��3������2�У������¶ȼƶ�����105�����ҵ�ԭ�����¶ȹ��Ͳ���������Ӧ�����ɵ�ˮ���¶ȹ���δ��Ӧ������������
��4���жϷ�Ӧ�ѻ�����ȫ�ķ���Ϊ��ƿ������ˮ���ӣ�
��5������3�г��Ƚ�����ﵹ��ʢ����ˮ���ձ��У������ȡ���ԭ�������÷�Ӧ�������ȴ�����������մ��ƿ���ϲ��״�����
��6������4�дֲ�Ʒ��һ���ᴿ�����ᴿ�������ؽᾧ��
��7������ʵ��IJ���Ϊ80%��
| A�� | 480mL����ƿ��7.68g����ͭ | B�� | 480mL����ƿ��12.0g���� | ||
| C�� | 500mL����ƿ��12.5g����ͭ | D�� | 500mL����ƿ��12.5g���� |
 ��1��ʵ��������ͼ��ʾװ���Ʊ���������������
��1��ʵ��������ͼ��ʾװ���Ʊ���������������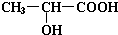 ���Իش�
���Իش�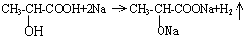 ��
��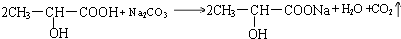 ��
�� ������ͭ�Ǻϳ��������������в���--��������ͭ����Ҫǰ����֮һ������������һ��ʵ���Һϳ�·�ߣ�
������ͭ�Ǻϳ��������������в���--��������ͭ����Ҫǰ����֮һ������������һ��ʵ���Һϳ�·�ߣ�