题目内容
19.下列各组离子在指定溶液中一定能大量共存的是( )| A. | pH=1的溶液中:Mg2+,CO${\;}_{3}^{2-}$,SO${\;}_{4}^{2-}$,Na+ | |
| B. | c(Fe3+)=0.1mol•L-1的溶液中:K+,SO${\;}_{4}^{2-}$,OH- | |
| C. | 使石蕊试液变蓝色的溶液中:Mg2+,Cl-,K+ | |
| D. | 使酚酞变红的溶液中:Na+,Cl-,SO${\;}_{4}^{2-}$ |
分析 A.pH=1的溶液呈酸性,与氢离子反应的离子不能大量共存;
B.与Fe3+反应的离子不能大量共存;
C.使石蕊试液变蓝色的溶液呈碱性,与OH-反应的离子不能大量共存;
D.使酚酞变红的溶液呈碱性.
解答 解:A.pH=1的溶液呈酸性,酸性条件下,CO32-不能大量共存,故A错误;
B.OH-与Fe3+反应生成沉淀,不能大量共存,故B错误;
C.使石蕊试液变蓝色的溶液呈碱性,Mg2+与OH-反应生成沉淀而不能大量共存,故C错误;
D.使酚酞变红的溶液呈碱性,离子之间不发生任何反应,可大量共存,故D正确.
故选D.
点评 本题考查离子共存问题,为高频考点,和常见题型,侧重于元素化合物知识的综合理解和运用的考查,注意把握题给信息以及隐含条件,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.有四种相同浓度的溶液:①甲酸、②碳酸、③醋酸、④石炭酸.它们的酸性由强到弱的是( )
| A. | ①③④② | B. | ①③②④ | C. | ④③②① | D. | ③①④② |
14.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,18g H20体积为22.4L | |
| B. | 2L 0.5mol/L CH3COOH溶液中含有的H+的数目为NA | |
| C. | 0.1mol锌与足量稀硫酸反应,转移的电子数为0.1NA | |
| D. | 常温常压下4.6g NO2与N2O4的混合气体,原子数为0.3NA |
4. 如图所示为离子化合物硼化镁的晶体结构单元,该化合物的化学式可以表示为( )
如图所示为离子化合物硼化镁的晶体结构单元,该化合物的化学式可以表示为( )
 如图所示为离子化合物硼化镁的晶体结构单元,该化合物的化学式可以表示为( )
如图所示为离子化合物硼化镁的晶体结构单元,该化合物的化学式可以表示为( )| A. | MgB2 | B. | Mg5B2 | C. | Mg7B3 | D. | MgB |
11.下表是四种弱酸常温下的电离平衡常数.
(1)多元弱酸的二级电离程度远小于一级电离的原因是多元弱酸一级电离生成的氢离子会抑制二级电离;
(2)HA、H2B、H2C、H3D四种酸中酸性最强的是H3D,最弱的是H2C;
(3)向10mL 0.01mol/L Na2B溶液中逐滴加入10mL 0.01mol/L HA溶液,并充分搅拌,反应的离子方程式是B2-+HA=HB-+A-;
(4)将等物质的量的HA、H2B、H2C、NaH2D溶于水配成混合溶液,若逐滴加入烧碱溶液,这四种物质中最先与烧碱反应的离子方程式是H3D+OH-=H2O+H2D-,若加入足量的烧碱溶液,最后与OH-反应的离子是HD2-+OH-=H2O+D3-.
| HA | H2B | H2C | H3D |
| 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
(2)HA、H2B、H2C、H3D四种酸中酸性最强的是H3D,最弱的是H2C;
(3)向10mL 0.01mol/L Na2B溶液中逐滴加入10mL 0.01mol/L HA溶液,并充分搅拌,反应的离子方程式是B2-+HA=HB-+A-;
(4)将等物质的量的HA、H2B、H2C、NaH2D溶于水配成混合溶液,若逐滴加入烧碱溶液,这四种物质中最先与烧碱反应的离子方程式是H3D+OH-=H2O+H2D-,若加入足量的烧碱溶液,最后与OH-反应的离子是HD2-+OH-=H2O+D3-.
14.葡萄糖酸钙是一种可促进骨骼生长的营养物质.葡萄糖酸钙可通过以下反应制得:
CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
实验流程如下:
葡萄糖溶液滴加3%溴水/55℃:①过量CaCO3/70℃②趁热过滤 ③乙醇 ④悬浊液
抽滤⑤洗涤⑥干燥⑦Ca(C6H11O7)2
葡萄糖溶液$→_{①}^{滴加3%溴水/55℃}$ $\underset{\stackrel{过量CaC{O}_{3}/70℃}{→}}{②}$ $→_{③}^{趁热过滤}$ $→_{④}^{乙醇}$ 悬浊液$→_{⑤}^{抽滤}$ $→_{⑥}^{洗涤}$$→_{⑦}^{干燥}$Ca(C6H11O7)2
请回答下列问题:
(1)第 ①步中溴水氧化葡萄糖时,下列装置最合适的是B(填序号).
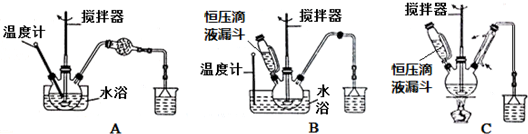
(2)第 ②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率,且过量的碳酸钙易除去.
(3)本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应制得葡萄糖酸钙.
(4)第 ③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤或损失产品.
(5)葡萄糖溶液与新制Cu(OH)2悬浊液反应的化学方程式为CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2OH(CHOH)4COONa+Cu2O↓+3H2O.
CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
葡萄糖溶液滴加3%溴水/55℃:①过量CaCO3/70℃②趁热过滤 ③乙醇 ④悬浊液
抽滤⑤洗涤⑥干燥⑦Ca(C6H11O7)2
葡萄糖溶液$→_{①}^{滴加3%溴水/55℃}$ $\underset{\stackrel{过量CaC{O}_{3}/70℃}{→}}{②}$ $→_{③}^{趁热过滤}$ $→_{④}^{乙醇}$ 悬浊液$→_{⑤}^{抽滤}$ $→_{⑥}^{洗涤}$$→_{⑦}^{干燥}$Ca(C6H11O7)2
请回答下列问题:
(1)第 ①步中溴水氧化葡萄糖时,下列装置最合适的是B(填序号).

(2)第 ②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率,且过量的碳酸钙易除去.
(3)本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应制得葡萄糖酸钙.
(4)第 ③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤或损失产品.
(5)葡萄糖溶液与新制Cu(OH)2悬浊液反应的化学方程式为CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2OH(CHOH)4COONa+Cu2O↓+3H2O.