题目内容
元素X、Y、Z在周期表中的相对位置如图所示.
已知Y元素原子的外围电子排布为ns(n-1)np(n+1),则下列说法不正确的是( )
| X | ||
| Y | ||
| Z |
| A、Y元素原子的外围电子排布为4s24p4 |
| B、Y元素在周期表的第三周期ⅥA族 |
| C、X元素所在周期中所含非金属元素最多 |
| D、Z元素的最高正价为+5价 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:Y元素原子的外围电子排布为ns(n-1)np(n+1),s能级最多容纳2个电子,故n-1=2,解得n=3,故Y元素原子的外围电子排布为3s23p4,Y为S元素,由X、Y、Z在周期表中的位置可知,X为F元素,Z为As元素,以此解答该题.
解答:
解:Y元素原子的外围电子排布为ns(n-1)np(n+1),s能级最多容纳2个电子,故n-1=2,解得n=3,故Y元素原子的外围电子排布为3s23p4,Y为S元素,由X、Y、Z在周期表中的位置可知,X为F元素,Z为As元素,
A.Y元素原子的外围电子排布为ns(n-1)np(n+1),s能级最多容纳2个电子,故n-1=2,解得n=3,故Y元素原子的外围电子排布为3s23p4,故A错误;
B.Y为S元素,处于第三周期第ⅥA族,故B正确;
C.X为F元素,处于第二周期,只有2两种金属元素,含有6种非金属元素,含非金属元素最多,故C正确;
D.Z为As元素,是33号元素,位于ⅤA族,最高正价为+5价,故D正确.
故选A.
A.Y元素原子的外围电子排布为ns(n-1)np(n+1),s能级最多容纳2个电子,故n-1=2,解得n=3,故Y元素原子的外围电子排布为3s23p4,故A错误;
B.Y为S元素,处于第三周期第ⅥA族,故B正确;
C.X为F元素,处于第二周期,只有2两种金属元素,含有6种非金属元素,含非金属元素最多,故C正确;
D.Z为As元素,是33号元素,位于ⅤA族,最高正价为+5价,故D正确.
故选A.
点评:本题考查结构与位置关系、核外电子排布规律、元素周期表等,难度不大,推断Y元素是解题的关键,注意基础知识的掌握.

练习册系列答案
相关题目
将淀粉氯化钾混合溶液装在羊皮纸制成的半透膜袋中,将此袋下半部浸泡在盛有蒸馏水的烧杯里,过一段时间后进行实验.下列现象能证明羊皮纸袋一定有破损的是( )
| A、取羊皮纸袋内液体加入碘水变蓝色 |
| B、取烧杯中液体加入KI溶液不变蓝色 |
| C、取烧杯中液体加入AgNO3溶液产生黄色沉淀 |
| D、取烧杯中液体加入碘水变蓝色 |
下列说法正确的是( )
| A、C2H4和C2H4O无论以何种比例混合,只要混合物总质量不变,完全燃烧时生成水的质量也不变 |
| B、分子式为C8H10且分子中有苯环的有机物共有3种 |
| C、汽油、柴油、植物油和甘油都是碳氢化合物 |
| D、溴苯分子中的所有原子都处在同一平面 |
下列各物质的溶液物质的量浓度均为0.1mol/L:①HCl;②NaOH;③Na2CO3;④NH4Cl;⑤CH3COONa;⑥Ba(OH)2;⑦KCl.它们pH按由小到大的排列顺序为( )
| A、⑥②③⑤⑦④① |
| B、①④⑦③⑤②⑥ |
| C、①④⑤③⑦②⑥ |
| D、①④⑦⑤③②⑥ |
下列反应属于放热反应的是( )
| A、铁与盐酸反应 |
| B、C与CO2共热 |
| C、碳酸钙的分解 |
| D、Ba(OH)2?8H2O晶体与NH4Cl晶体反应 |
英国物理学家约翰?丁达尔首先发现了入射光透过胶体时,从侧面可以看到一条光亮的通路.下列液体中,不会出现丁达尔效应的分散系的是( )①鸡蛋白溶液 ②肥皂水 ③淀粉溶液 ④硝酸钾溶液.
| A、① | B、② | C、④ | D、③ |
在相同条件下,下列气体中密度最大的是( )
| A、H2 |
| B、O2 |
| C、C12 |
| D、HCl |
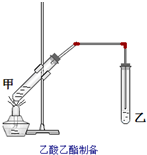 如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5mL饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答: