题目内容
a mol N2与b mol H2混合,要一定条件下反应达到平衡,生成了c mol NH3,则NH3在平衡体系中质量分数为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:化学方程式的有关计算
专题:计算题
分析:由质量守恒可知,平衡后混合气体总质量等于开始时N2、H2的总质量,根据m=nM计算NH3的质量、混合气体总质量,进而计算氨气质量分数.
解答:
解:由质量守恒可知,平衡后混合气体总质量等于开始时N2、H2的总质量,即混合气体总质量为amol×28g/mol+b mol×2g/mol=(28a+2b)g,
NH3的质量为c mol×17g/mol=17c g,
故平衡混合气体中氨气质量分数为
×100%=
×100%.
NH3的质量为c mol×17g/mol=17c g,
故平衡混合气体中氨气质量分数为
| 17cg |
| ((28a+2b)g |
| 17c |
| 28a+2b |
点评:本题考查物质的量有关计算,比较基础,注意根据质量守恒定律计算平衡后混合气体总质量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知下列热化学方程式:
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.31kJ/mol
②2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=-3119.6kJ/mol
③C2H4(g)+3O2(g)═2CO2(g)+2H2O(l)△H=-1411.0kJ/mol
④2C2H2(g)+5O2 (g)═4CO2(g)+2H2O(l)△H=-2599.2kJ/mol
⑤C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2219.9kJ/mol
现有由2mol上述五种烃中的两种组成的气体混合物,经充分燃烧后放出3037kJ热量,则下列组合中不可能的是( )
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.31kJ/mol
②2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=-3119.6kJ/mol
③C2H4(g)+3O2(g)═2CO2(g)+2H2O(l)△H=-1411.0kJ/mol
④2C2H2(g)+5O2 (g)═4CO2(g)+2H2O(l)△H=-2599.2kJ/mol
⑤C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2219.9kJ/mol
现有由2mol上述五种烃中的两种组成的气体混合物,经充分燃烧后放出3037kJ热量,则下列组合中不可能的是( )
| A、C2H4和C2H6 |
| B、C2H2和C3H8 |
| C、C2H6和C3H8 |
| D、C2H6和CH4 |
下列说法正确的是( )
| A、乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | ||
| B、分子式为C4H7ClO2可与NaHCO3产生CO2,可能结构有3种 | ||
C、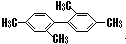 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 | ||
D、用
|
某双原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏加德罗常数为NA,则:
(1)该气体的物质的量为 mol.
(2)该气体所含原子总数为 个.
(3)该气体的一个分子的质量为 g.
(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体的一个分子的质量为
向100mL18mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应,再加入足量的锌片,充分反应后,被还原的H2SO4的物质的量( )
| A、小于0.9mol |
| B、等于0.9mol |
| C、在0.9mol与1.8mol之间 |
| D、等于1.8mol |
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛,因而称为释迦牟尼分子,有关该有机分子的说法正确的是( )
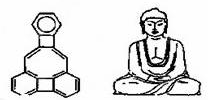

| A、该有机物所有原子一定在同一平面 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子中含有21个碳原子 |
| D、该有机物一氯代物只有4种 |