题目内容
3.有pH均为2的盐酸、硫酸和醋酸三种溶液,①若分别用这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积分别为a、b、c,则它们的大小关系是a=b>c;
②若在相同条件下和碳酸钠反应产生的气体体积分别是a、b、c,则它们的大小关系是a=b<c.
③盐酸中c(Cl-)与醋酸中c(CH3COO-)的大小关系是c(Cl-)=c(CH3COO-).
分析 ①pH均为2的盐酸、硫酸中和碱的能力相同,醋酸是弱酸部分电离,酸的浓度大于氢离子浓度;
②pH均为2的盐酸、硫酸中氢离子浓度相同,醋酸中氢离子被消耗还能继续电离氢离子;
③根据电荷守恒分析.
解答 解:①pH均为2的盐酸、硫酸中和碱的能力相同,中和含等物质的量NaOH的溶液,需要的硫酸和盐酸的体积相同,醋酸是弱酸部分电离,酸的浓度大于氢离子浓度,中和含等物质的量NaOH的溶液,消耗的醋酸的体积最小,所以a=b>c;
故答案为:a=b>c;
②pH均为2的盐酸、硫酸中氢离子浓度相同,与碳酸钠反应产生的气体体积相同,醋酸中氢离子被消耗还能继续电离氢离子,醋酸的浓度大于氢离子的浓度,而盐酸的浓度等于氢离子的浓度,所以醋酸的浓度大于盐酸的浓度,因此,醋酸与碳酸钠反应生成的气体的体积大,则a=b<c;
故答案为:a=b<c;
③pH均为2的盐酸、醋酸,氢离子浓度均为10-2mol/L,溶液中的电荷守恒为c(H+)=c(Cl-)+c(OH-),c(H+)=c(CH3COO-)+c(OH-),两个溶液中c(H+)、c(OH-)均相同,所以c(Cl-)=c(CH3COO-);
故答案为:c(Cl-)=c(CH3COO-).
点评 本题考查电解质的电离,题目难度中等,侧重于考查学生的分析能力和对基础知识的应用能力,注意弱电解质溶液中pH与弱电解质浓度的关系.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
13. 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)800℃,反应达到平衡时,NO的物质的量浓度是0.0035mol/L;升高温度,NO的浓度增大,则该反应是放热(填“放热”或“吸热”)反应.
(2)如图中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol/(L•s).
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图中表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol/(L•s).
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变.
11.下列物质不能用水加以鉴别的是( )
| A. | 苯和四氯化碳 | B. | 氢氧化钠固体和食盐 | ||
| C. | 石灰石和重晶石 | D. | 酒精和汽油 |
18.下列叙述不正确的是( )
| A. | 氨水中:c(NH3•H2O)>c(NH${\;}_{4}^{+}$)>c(OH-) | |
| B. | 饱和H2S溶液中:c(H2S)>c(H+)>c(HS-)>c(S2-) | |
| C. | 0.1mol/LCH3COOH溶液中:c(H+)-c(OH-)=c(CH3COO-) | |
| D. | NaOH溶液中:c(H+)+c(Na+)=c(OH-) |
8.下列反应不属于氧化还原反应的是( )
| A. | 铝片与稀盐酸的反应 | B. | Ca(OH)2与NH4Cl的反应 | ||
| C. | 灼热的炭与CO2的反应 | D. | 甲烷在氧气中的燃烧反应 |
15.下列实验操作正确的是( )
| A. | 用酒精萃取碘水中的碘 | |
| B. | 蒸馏时,应使温度计水银球伸入蒸馏烧瓶内液面下 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定不含有K+ |
12.下列说法正确的是( )
| A. | 铝有较高熔点,可做耐火材料 | |
| B. | SO2能使溴水褪色,体现其漂白性 | |
| C. | 氨气是电解质,因为氨气的水溶液能导电 | |
| D. | 钠钾合金可用于快中子反应堆的热交换剂 |
13.下列有关化学用语表达正确的是( )
| A. | 质子数为92、中子数为146的U原子:${\;}_{92}^{146}$U | |
| B. | HClO的结构式:H-Cl-O | |
| C. | HF的电子式: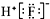 | |
| D. | 35Cl-和37Cl-离子结构示意图均可以表示为: |