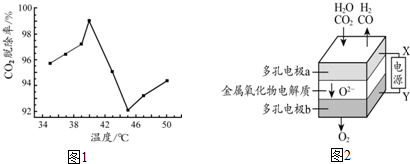
题目内容
4.下列实验操作正确的是( )| A. | 分液操作时分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| B. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液小火加热蒸干 | |
| C. | 利用蒸馏的方法进行乙醇与水的分离时,温度计水银球应放在液面以下来准确测定温度 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
分析 A.分液操作时下层液体从下口放出,上层液体从上口倒出;
B.蒸发皿中溶液析出大量固体时停止加热,用余热将固体蒸干;
C.蒸馏时,温度计测量馏分温度;
D.萃取剂的选择与密度无关.
解答 解:A.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,一避免两种液体相互污染,故A正确;
B.用蒸发方法使NaCl从溶液中析出时,应加热至蒸发皿中溶液析出大量固体时停止加热,用余热将固体蒸干,故B错误;
C.蒸馏是用来分离沸点不同的液体混合物,温度计测量的是蒸汽的温度,故应放在支管口,故C错误;
D.萃取剂的密度不一定比水大,只要符合萃取剂与原溶剂互不相溶,溶质在萃取剂中的溶解度比在水中大即可,故D错误.
故选A.
点评 本题考查较为综合,涉及基础实验操作,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.将某元素形成的单质0.1mol与氯气充分反应,生成物的质量比原单质的质量增加了7.1g,这种元素可能是( )
| A. | Na | B. | Fe | C. | Cu | D. | Al |
17.化学与科技、生活、资源的综合利用、环境密切相关,下列说法不正确的是( )
| A. | 煤的综合利用主要是煤的干馏、液化和气化,气化是指:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2 | |
| B. | 高温结构陶瓷氮化硅(Si3N4),属于新型无机非金属材料,可用于制造汽车发动机 | |
| C. | 用铝质铆钉来焊接铁板,铁板易被腐蚀 | |
| D. | 用铜、稀硫酸、过氧化氢混合制硫酸铜法体现了“绿色化学”的思想 |
4.某有机物的分子式为C4H10O,则其同分异构体中( )
| A. | 醚有2种,醇有3种 | B. | 醚有3种,醇有3种 | C. | 醚有3种,醇有4种 | D. | 醚有2种,醇有4种 |
9.下列判断正确的是( )
| A. | 同体积、同浓度的NaF和NaCl溶液中,所有离子总数,N(NaCl)>N(NaF);同体积同浓度的Na2CO3和Na2SO4溶液中,所有离子总数,N(Na2CO3)>N(Na2SO4) | |||||||||||
| B. | 以下是某温度下高氯酸、硫酸、硝酸和盐酸在冰醋酸中的电离常数,则在冰醋酸中硫酸的电离方程式可表示为H2SO4?2H++SO42-
| |||||||||||
| C. | 已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,[c(Na+)-c(F-)]<[c(K+)-c(CH3COO-)] | |||||||||||
| D. | 平衡体系CaCO3(s)?CaO(s)+CO2中仅含有碳酸钙、氧化钙及二氧化碳气体.某时刻,保持温度不变,将容器体积缩小为原来的一半并保持不变,则二氧化碳浓度增大 |
16.如图所示的实验方法、装置或操作完全正确的是( )
| A. |  稀释浓H2SO4 | B. |  萃取时振荡 | ||
| C. |  石油的蒸馏 | D. | 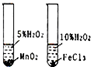 验证催化剂的效果 |
13.下列有机反应属于加成反应的是( )
| A. | CH4+Cl2$\stackrel{光}{→}$ CH3Cl+HCl | |
| B. | CH3CH2OH+CH3COOH $→_{△}^{浓硫酸}$ CH3COOCH2CH3+H2O | |
| C. | H2C=CH2+HCl→H2C-CH2Cl | |
| D. | 2CH3CH2OH+O2 $→_{△}^{Cu}$ 2CH3CHO+2H2O |