题目内容
1L质量分数为98%(密度为1.84g/cm3)的浓硫酸中含 mol的硫酸分子,含 mol的氧原子,含 克氢元素.
考点:物质的量的相关计算
专题:计算题
分析:根据m=ρV计算溶液的质量,再根据m(溶质)=m(溶液)×ω计算硫酸的质量,根据n=
计算硫酸的物质的量;氧原子物质的量为硫酸的4倍,氢原子物质的量为硫酸的2倍,根据m=nM计算氢元素质量.
| m |
| M |
解答:
解:溶液质量为1000mL×1.84g/mL=1840g,
故溶质硫酸的质量=1840g×98%,
则硫酸的物质的量=
=18.4mol,
氧原子物质的量为硫酸的4倍,含有氧原子物质的量=18.4mol×4=73.6mol,
氢原子物质的量为硫酸的2倍,含有氢原子物质的量=18.4mol×2=36.8mol,则氢元素质量=36.8mol×1g/mol=36.8g,
故答案为:18.4;73.6; 36.8.
故溶质硫酸的质量=1840g×98%,
则硫酸的物质的量=
| 1840g×98% |
| 98 |
氧原子物质的量为硫酸的4倍,含有氧原子物质的量=18.4mol×4=73.6mol,
氢原子物质的量为硫酸的2倍,含有氢原子物质的量=18.4mol×2=36.8mol,则氢元素质量=36.8mol×1g/mol=36.8g,
故答案为:18.4;73.6; 36.8.
点评:本题考查质量分数计算、物质的量有关计算,掌握公式即可解答,有利于基础知识的巩固.

练习册系列答案
相关题目
下列描述中,不符合生产实际的是( )
| A、电解法精炼粗铜,用纯铜作阴极 |
| B、在镀件上电镀锌,用锌作阳极 |
C、 用如图装置生产家用消毒液(NaClO) |
D、 用如图装置为铅蓄电池充电 |
高一入学体检时,小明体检的血液化验单中,出现了如下所示的体检指标.表示该体检指标的物理量是( )
甘油三酯 0.52 mmol/L; 总胆固醇 4.27 mmol/L.
甘油三酯 0.52 mmol/L; 总胆固醇 4.27 mmol/L.
| A、溶解度 | B、物质的量浓度 |
| C、质量分数 | D、摩尔质量 |
化学与资源、环境、生活关系密切,下列说法不正确的是( )
| A、处理废水时可加入明矾作为混凝剂,以吸附水中的杂质 |
| B、废弃的塑料、金属、纸制品是可回收资源,玻璃是不可回收资源 |
| C、酸雨样品露天放置一段时间,酸性增强,是由于雨水中某种成分被氧化 |
| D、工业上可利用铝热反应原理制备高熔点金属 |


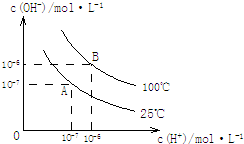 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示: