题目内容
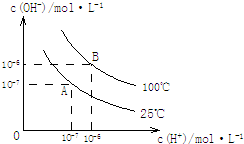 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:(1)A点水的离子积为1×10-14,B点水的离子积为
(2)25℃时,H2R在水溶液中的电离方程式为:H2R=H++HR-,HR-?H++R2-
①0.1mol/LH2R溶液的pH
②在0.1mol/LNaHR溶液中,各离子浓度由大到小的顺序是:
(3)100℃时,0.01mol/LNaOH溶液的pH=
(4)100℃时,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为
考点:pH的简单计算,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)c(H+).c(OH-)=Kw,水的电离是吸热反应,升高温度促进电离;
(2)①由H2R的电离方程式可知0.1mol/LH2R溶液中氢离子浓度大于0.1mol/L;
②由H2R的电离方程式可知HR-的电离程度大于水解程度;
(3)c(OH-)=0.01mol/L=
、pH=-lgc(H+).
(4)先根据水的离子积常数计算氢氧化钡溶液中c(OH-),再根据盐酸和氢氧化钡之间的关系计算氢氧化钡和盐酸的体积之比.
(2)①由H2R的电离方程式可知0.1mol/LH2R溶液中氢离子浓度大于0.1mol/L;
②由H2R的电离方程式可知HR-的电离程度大于水解程度;
(3)c(OH-)=0.01mol/L=
| Kw |
| c(H+) |
(4)先根据水的离子积常数计算氢氧化钡溶液中c(OH-),再根据盐酸和氢氧化钡之间的关系计算氢氧化钡和盐酸的体积之比.
解答:
解:(1)c(H+).c(OH-)=Kw=10-6×10-6=10-12,水的电离要吸热,温度升高,水的电离程度增大,即离子积增大,
故答案为:10-12;水的电离要吸热,温度升高,水的电离程度增大,即离子积增大;
(2)①由H2R的电离方程式可知0.1mol/LH2R溶液中氢离子浓度大于0.1mol/L,因此PH小于1,
故答案为:<;
②由H2R的电离方程式可知HR-的电离程度大于水解程度,因此溶液呈酸性,c(OH-)最小,HR-的电离和水解均减小了其浓度,因此c(Na+)>c(HR-),电离和水解程度较弱,所以c(HR-)>c(H+),因此离子浓度大小顺序为c(Na+)>c(HR-)>c(H+)>c(R2-)>c(OH-),
故答案为:c(Na+)>c(HR-)>c(H+)>c(R2-)>c(OH-);
(3)0.01mol/LNaOH溶液c(OH-)=0.01mol/L,c(H+)=
=
mol/L=10-10 mol/L,带入pH=-lgc(H+)=10,
故答案为:10;
(4)将pH=8的Ba(OH)2溶液中c(OH-)=10-4 mol/L,pH=5的稀盐酸中c(H+)=10-5 mol/L,
设氢氧化钡的体积为x,盐酸的体积为y,100℃的恒温,欲使混合溶液pH=7,溶液呈碱性,
c(OH-)=
mol/L=10-5 mol/L,c(OH-)=
=10-5 mol/L,解得x:y=2:9,
故答案为:2:9.
故答案为:10-12;水的电离要吸热,温度升高,水的电离程度增大,即离子积增大;
(2)①由H2R的电离方程式可知0.1mol/LH2R溶液中氢离子浓度大于0.1mol/L,因此PH小于1,
故答案为:<;
②由H2R的电离方程式可知HR-的电离程度大于水解程度,因此溶液呈酸性,c(OH-)最小,HR-的电离和水解均减小了其浓度,因此c(Na+)>c(HR-),电离和水解程度较弱,所以c(HR-)>c(H+),因此离子浓度大小顺序为c(Na+)>c(HR-)>c(H+)>c(R2-)>c(OH-),
故答案为:c(Na+)>c(HR-)>c(H+)>c(R2-)>c(OH-);
(3)0.01mol/LNaOH溶液c(OH-)=0.01mol/L,c(H+)=
| Kw |
| c(OH-) |
| 10-12 |
| 0.01 |
故答案为:10;
(4)将pH=8的Ba(OH)2溶液中c(OH-)=10-4 mol/L,pH=5的稀盐酸中c(H+)=10-5 mol/L,
设氢氧化钡的体积为x,盐酸的体积为y,100℃的恒温,欲使混合溶液pH=7,溶液呈碱性,
c(OH-)=
| 10-12 |
| 10-7 |
| 10-4x-10-5y |
| x+y |
故答案为:2:9.
点评:本题考查了离子浓度的大小比较、pH以及离子积常数的有关计算,注意混合溶液的pH=7时溶液呈碱性而不是中性,为易错点.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列化学反应的产物中,存在同分异构体的是( )
| A、乙烯与溴化氢加成 |
| B、CH3CH2CH2Br与NaOH水溶液共热 |
| C、丙烯与氯气加成 |
| D、CH3CHBrCH2CH3与NaOH醇溶液共热 |
 镍锌电池具有绿色环保、大电流、性能好等优点,是电动玩具和数码产品的理想电源,如图是其工作原理示意图.下列说法正确的是( )
镍锌电池具有绿色环保、大电流、性能好等优点,是电动玩具和数码产品的理想电源,如图是其工作原理示意图.下列说法正确的是( )| A、a为电池负极,电池放电时发生还原反应 |
| B、电池放电时,负极附近区域pH升高 |
| C、电池充电时,阳极反应为2Ni(OH)2-2e-+2OH-═2NiOOH+2H2O |
| D、电池充电时,总反应为Zn+2NiOOH+H2O═ZnO+2Ni(OH)2 |
 (1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料.如LiFePO4电池中某电极的工作原理如图:
(1)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力.锂是制造化学电源的重要原料.如LiFePO4电池中某电极的工作原理如图: