题目内容
4.已知CH30H(1)的燃烧热为-726kJ•mol-1下列对于反应2CH30H(1)+3O2(g)═2CO2(g)+4H2O(?)△H=-1452kJ•mol-1中水的状态判断正确的是( )| A. | 气态 | B. | 液态 | C. | 固态 | D. | 无法判断 |
分析 燃烧热是指在101KP时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,此时C需转化为二氧化碳,H需转化为液态水.CH30H(1)的燃烧热为-726kJ•mol-1,即1molCH30H(1)当完全燃烧生成二氧化碳气体和液态水时,放热726kJ,故可得出2molCH30H(1)完全燃烧生成二氧化碳气体和液态水时,放出热量的数值,与所给的热化学方程式中的相比较,得出结论.
解答 解:燃烧热是指在101KP时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,此时C需转化为二氧化碳,H需转化为液态水.
由于CH30H(1)的燃烧热为-726kJ•mol-1,即1molCH30H(1)当完全燃烧生成二氧化碳气体和液态水时,放热726kJ,故可得出2molCH30H(1)完全燃烧生成二氧化碳气体和液态水时,放出热量的数值为1452kJ,与所给的热化学方程式中的相符,故热化学方程式中生成的水应为液态,故选B.
点评 本题考查了燃烧热的概念和注意事项,应注意的是燃烧热是指在101KP时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,此时C需转化为二氧化碳,H需转化为液态水,难度不大.

练习册系列答案
相关题目
14.下列各式用电子式表示的物质的形成过程,其中正确的是( )
| A. | 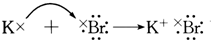 | |
| B. | 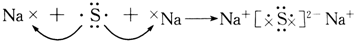 | |
| C. | 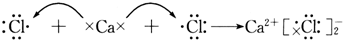 | |
| D. | 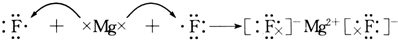 |
19.一般烃分子脱去两个氢原子形成烯键是吸热反应,脱氢形成双键约需112kJ/mol~125kJ/mol的热量.但是1,3-环己二烯( )脱氢生成苯是放热反应,反应约为23.4kJ/mol,此事实能说明( )
)脱氢生成苯是放热反应,反应约为23.4kJ/mol,此事实能说明( )
 )脱氢生成苯是放热反应,反应约为23.4kJ/mol,此事实能说明( )
)脱氢生成苯是放热反应,反应约为23.4kJ/mol,此事实能说明( )| A. | 1,3-环己二烯加氢是吸热反应 | |
| B. | 1,3-环己二烯的碳架变为苯环后,并不是简单的形成一个新的双键,而是具有了一个特殊稳定结构 | |
| C. | 1,3-环己二烯不及苯稳定 | |
| D. | 1,3-环己二烯加氢生成环己烷是吸热反应 |
9.下列叙述正确的是( )
| A. | 溶液是无色透明的、均一的、稳定的混合物 | |
| B. | 浊液很不稳定,分散质颗粒在重力的作用下一定会向下沉淀 | |
| C. | 胶体在一定条件下能稳定住,属于稳定系 | |
| D. | 植物油溶入汽油中形成的分散系,为不稳定的乳浊液 |
16.NA为阿伏伽德罗常数,下列物质所含分子数最大的是( )
| A. | 0.6mol酒精 | B. | 标准状况下4.48L SO2 | ||
| C. | 0.36g H2O | D. | 含NA个氢原子的甲烷 |
14.2000年诺贝尔化学奖授予两位美国化学家和一位日本化学家,以表彰他们在导电塑料领域的贡献,他们首先把聚乙炔树脂制成导电塑料.下列关于聚乙炔的叙述错误的是( )
| A. | 聚乙炔是乙炔发生聚合反应形成的高聚物 | |
| B. | 聚乙炔的化学式为 | |
| C. | 聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质 | |
| D. | 等质量的聚乙炔和乙烯分别完全燃烧时,它们耗氧量相同 |
15.室温下,有pH=3的盐酸、硫酸、醋酸(假设醋酸有1%的电离)三种相同体积的溶液.以下叙述错误的是( )
| A. | 溶液的导电性能相同 | |
| B. | 与足量的锌粉反应的起始速率相同 | |
| C. | 与足量的锌粉反应产生氢气的体积比为1:2:100 | |
| D. | 与同浓度氢氧化钠溶液反应,消耗氢氧化钠溶液的体积为1:1:100 |