题目内容
3.A、B、C、D、E、F六种物质含有同一种元素,六种物质的相互转化关系如下,E是淡黄色粉末,判断: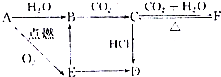
写出有关反应的化学方程式(是离子反应的直接写出离子方程式)
B→C:2OH-+CO2=CO32-+H2O; E→B:2Na2O2+2H2O=4Na++4OH-+O2↑;
C→F:CO32-+H2O+CO2=2HCO3-; F→C:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
分析 A与氧气反应生成淡黄色粉末E为Na2O2,则A为Na,钠与水反应生成B且也能由过氧化钠转化得到,可推知B为NaOH,由于NaOH与二氧化碳得到C,C与二氧化碳、水反应得到F,可推知C为Na2CO3、F为NaHCO3,碳酸钠与HCl反应得到固体D,且能由过氧化钠转化得到,可推知D为NaCl,据此解答.
解答 解:A与氧气反应生成淡黄色粉末E为Na2O2,则A为Na,钠与水反应生成B且也能由过氧化钠转化得到,可推知B为NaOH,由于NaOH与二氧化碳得到C,C与二氧化碳、水反应得到F,可推知C为Na2CO3、F为NaHCO3,碳酸钠与HCl反应得到固体D,且能由过氧化钠转化得到,可推知D为NaCl,
(1)由上述分析可知,A为Na,D为NaCl,故答案为:Na;NaCl;
(2)B→C是氢氧化钠与二氧化碳反应生成碳酸钠与水,反应离子方程式为:2OH-+CO2=CO32-+H2O,
E→B是过氧化钠与水反应生成氢氧化钠与氧气,反应离子方程式为:2Na2O2+2H2O=4Na++4OH-+O2↑,
C→F是碳酸钠与二氧化碳、水反应生成碳酸氢钠,反应离子方程式为:CO32-+H2O+CO2=2HCO3-,
F→C是碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
故答案为:2OH-+CO2=CO32-+H2O;2Na2O2+2H2O=4Na++4OH-+O2↑;CO32-+H2O+CO2=2HCO3-,2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
点评 本题考查无机物推断,涉及钠元素单质及其化合物的转化,突破口为“E为淡黄色粉末及由A与氧气在点燃条件下得到”,再结合转化关系推断,难度不大,注意基础知识的掌握.

| A. | 盐酸 | B. | 蔗糖 | C. | 硫酸钠 | D. | 二氧化碳 |
| A. | c(H+)=1.0×10-12mol•L-1的溶液中:K+、AlO2-、NO3-、Na+ | |
| B. | pH=0的溶液:Fe2+、Br-、Na+、NO3- | |
| C. | 强酸性溶液中:Fe3+、K+、SCN-、SO42- | |
| D. | 石蕊试液呈紫色的溶液中:NH4+、Al3+、NO3-、HCO3- |
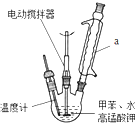 苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等.实验室合成苯甲酸的原理、有关数据及装置示意图如下:
苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等.实验室合成苯甲酸的原理、有关数据及装置示意图如下:反应过程:
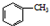 $→_{△}^{KMnO_{4}}$
$→_{△}^{KMnO_{4}}$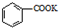 $\stackrel{HCl}{→}$
$\stackrel{HCl}{→}$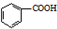
反应试剂、产物的物理常数:
| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 溶解度(g) | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.4[1] | 248 | 1.2659 | 微溶[2] | 易溶 |
[2]苯甲酸在100g水中的溶解度为:4℃,0.18g;18℃,0.27g;75℃,2.2g.
按下列合成步骤回答问题:
Ⅰ.苯甲酸制备:
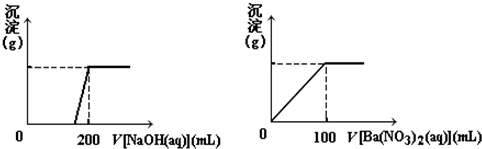
按如图在250mL三颈烧瓶中放入2.7mL甲苯和100mL水,控制100℃机械搅拌溶液,在石棉网上加热至沸腾.从冷
凝管上口分批加入8.5g高锰酸钾(加完后用少量水冲洗冷凝管内壁),继续搅拌约需4~5h,静置发现不再出
现分层现象时,停止反应.装置a的作用是将甲苯和水冷凝回流,防止甲苯的挥发而降低产品产率.写出并配平该反应化学方程式:

Ⅱ.分离提纯:
(1)除杂.将反应混合物加入一定量亚硫酸氢钠溶液使紫色褪去,此时反应的离子方程式为2MnO4-+3HSO3-+OH-=2MnO2↓+3SO42-+2 H2O.
(2)趁热过滤、热水洗涤.趁热过滤目的是除去二氧化锰并防止苯甲酸钾结晶析出造成损失.
(3)苯甲酸生成.合并实验(2)滤液和洗涤液,放在冰水浴中冷却,然后用浓盐酸酸化,至苯甲酸全部析出.将析出的苯甲酸减压过滤,得到滤液A和沉淀物B.沉淀物B用少量冷水洗涤,挤压去水分,把制得的苯甲酸放在水浴上干燥,得到粗产品C.
(4)粗产品提纯.将粗产品C进一步提纯,可用下列BD操作(填字母).
A.萃取分液 B.重结晶 C.蒸馏 D.升华
Ⅲ.产品纯度测定:称取1.220g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶,滴加2~3滴酚酞(填写“甲基橙”或“酚酞”),然后用0.1000mol•L-1KOH溶液滴定,到达滴定终点时消耗KOH溶液24.00mL.产品中苯甲酸质量分数为96.00%.
 随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视. 是一种具有较好耐热性、耐水性和高频电绝缘性的高分子化合物(树脂),它是由三种单体在一定条件下缩聚(同时还生成水)而成的.这三种单体分别是(写结构简式)C6H5NH2、HCHO和
是一种具有较好耐热性、耐水性和高频电绝缘性的高分子化合物(树脂),它是由三种单体在一定条件下缩聚(同时还生成水)而成的.这三种单体分别是(写结构简式)C6H5NH2、HCHO和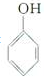 .它们的物质的量之比(按以上回答单体的顺序写)为1:2:1.
.它们的物质的量之比(按以上回答单体的顺序写)为1:2:1.