题目内容
(10分)如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
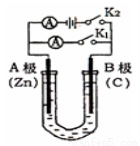
(1)打开K2,合并K1,若所盛溶液为CuSO4溶液:则A为 极,A极的电极反应式为 。若所盛溶液为KCl溶液:则B极的电极反应式为
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的NaCl溶液,则A电极附近可观察到的现象是 ,Na+移向 极(填A、B);B电极上的电极反应式为 ,总反应化学方程式是 。
(3)如果要用电解的方法精炼粗铜,打开K1,合并K2,电解液选用CuSO4溶液,则A电极的材料应换成是 (填“粗铜”或“纯铜”),电极反应式是 ,反应一段时间后电解质溶液中Cu2+的浓度将会 (填“增大”、“减小”、“不变”)。
(1)负;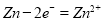 ;
;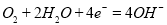 ;(2)有无色气体生成,溶液显红色;A;
;(2)有无色气体生成,溶液显红色;A;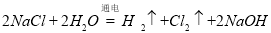 ;(3)纯铜;
;(3)纯铜;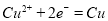 ;减小
;减小
【解析】
试题分析:打开K2,合并K1,该装置为原电池,锌为活泼金属,所以锌为负极,B极为正极;锌失电子发生氧化反应,电极反应式为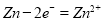 ;若所盛溶液为KCl溶液,锌发生吸氧腐蚀,则正极极的电极反应式为
;若所盛溶液为KCl溶液,锌发生吸氧腐蚀,则正极极的电极反应式为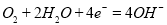 ;打开K1,合并K2,为电解池,若所盛溶液为滴有酚酞的NaCl溶液,电解池总反应为
;打开K1,合并K2,为电解池,若所盛溶液为滴有酚酞的NaCl溶液,电解池总反应为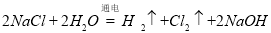 ;A极为阴极,极反应为
;A极为阴极,极反应为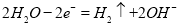 ,阴极区域溶液显碱性,溶液变红色。B为阳极,阳极反应式为
,阴极区域溶液显碱性,溶液变红色。B为阳极,阳极反应式为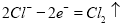 ;阳离子移向阴极;(3)电解的方法精炼粗铜粗铜作阳极,精铜作阴极,阳极反应主要为
;阳离子移向阴极;(3)电解的方法精炼粗铜粗铜作阳极,精铜作阴极,阳极反应主要为 ,可能有比铜活泼的金属(如铁、锌)失电子,阴极反应为,
,可能有比铜活泼的金属(如铁、锌)失电子,阴极反应为,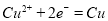 ;所以Cu2+的浓度减小。
;所以Cu2+的浓度减小。
考点:本题考查原电池、电解池、电解法精炼铜。

 2SO3(g),在不同条件下测得化学反应速率最快的为
2SO3(g),在不同条件下测得化学反应速率最快的为
 混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加____________g;此时,所有电极上总共收集到的气体的总体积为___________L(换算成标准状况下的体积)。
混合溶液,溶液体积为500ml,M、N均为石墨电极,当装置A中Zn棒质量减少6.5g时,N上质量增加____________g;此时,所有电极上总共收集到的气体的总体积为___________L(换算成标准状况下的体积)。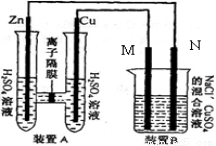
 2HI(g)的平衡常数是49,则
2HI(g)的平衡常数是49,则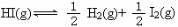 ,在该温度下的平衡常数是
,在该温度下的平衡常数是 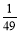 B.7 C.2401 D.
B.7 C.2401 D.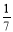
 2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(假定测量过程中没有能量损失):
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(假定测量过程中没有能量损失):