题目内容
下列分子中所有的原子都满足最外层为8电子结构的是( )
| A、BCl3 |
| B、COCl2 |
| C、SF6 |
| D、SiH4 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:对于ABn型共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,含H元素的化合物一定不满足8电子结构.
解答:
解:A、BCl3中,B元素位于第ⅢA族,则3+3≠8,不满足分子中所有原子都满足最外层8电子结构,故A错误;
B、光气(COCl2)中,C原子的原子核外最外层电子数为4,其在分子中的化合价为+4价,所以满足最外层8电子结构,O原子的原子核外最外层电子数为6,其在分子中的化合价为-2价,所以满足最外层8电子结构;Cl原子的原子核外最外层电子数为7,其在分子中的化合价为-1价,所以满足最外层8电子结构,故B正确;
C、SF5中S元素化合价为+6,S原子最外层电子数为6,所以6+6=12,S原子不满足8电子结构,F元素化合价为-1,F原子最外层电子数为7,所以1+7=8,F原子满足8电子结构,故C错误;
D、SiH4中Si元素化合价为+4,Si原子最外层电子数为4,所以4+4=8,Si原子满足8电子结构,H原子的最外层电子为:1+1=2,不都满足8电子稳定结构,故D错误.
故选:B.
B、光气(COCl2)中,C原子的原子核外最外层电子数为4,其在分子中的化合价为+4价,所以满足最外层8电子结构,O原子的原子核外最外层电子数为6,其在分子中的化合价为-2价,所以满足最外层8电子结构;Cl原子的原子核外最外层电子数为7,其在分子中的化合价为-1价,所以满足最外层8电子结构,故B正确;
C、SF5中S元素化合价为+6,S原子最外层电子数为6,所以6+6=12,S原子不满足8电子结构,F元素化合价为-1,F原子最外层电子数为7,所以1+7=8,F原子满足8电子结构,故C错误;
D、SiH4中Si元素化合价为+4,Si原子最外层电子数为4,所以4+4=8,Si原子满足8电子结构,H原子的最外层电子为:1+1=2,不都满足8电子稳定结构,故D错误.
故选:B.
点评:本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
相关题目
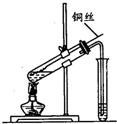 如图是实验室研究浓硫酸性质的实验,下列分析错误的是( )
如图是实验室研究浓硫酸性质的实验,下列分析错误的是( )| A、该实验说明浓硫酸具有强氧化性 |
| B、反应后试管中观察到的白色固体CuSO4 |
| C、该实验产生的气体不会造成环境污染,因此不需尾气处理 |
| D、实验结束,将铜丝拉离液面终止反应 |
 可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空:
可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空: