题目内容
20.氧元素可形成多种单质,也可与许多元素形成化合物,下列有关叙述正确的是( )| A. | 16O2、18O3互为同位素 | |
| B. | 次氯酸的电子式为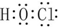 | |
| C. | 氧与氟形成的化合物(OF2)中,氧元素的化合价为-2价 | |
| D. | 一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
分析 A.有相同质子数,不同中子数的原子互为同位素;相同元素组成,不同形态的单质互为同素异形体;
B.次氯酸分子中中心原子是氧原子,其结构式为H-O-Cl;
C.氟的电负性大于氧,所以氟吸引电子的能力大于氧;
D.同种化合价对应的氧化物不一定只有一种.
解答 解:A.16O2、18O3都是由氧元素形成的不同单质,故互为同素异形体,故A错误;
B.次氯酸为共价化合物,H原子最外层1个电子,Cl原子最外层7个电子,O原子最外层6个电子,则其电子式为: ,故B正确;
,故B正确;
C.氟的电负性大于氧,所以氟吸引电子的能力大于氧,在氧与氟形成的化合物中氟显-1价,氧显+2价,其分子式为OF2,故C错误;
D.同种化合价对应的氧化物不一定只有一种,如+4价的氮元素的氧化物有NO2和N2O4,故D错误;
故选B.
点评 本题考查化学用语,题目难度不大,注意次氯酸电子式的书写,为易错点.

练习册系列答案
相关题目
11.通常用于金属制品表面防腐的“银粉”,实际上是下列哪种金属粉末( )
| A. | Al | B. | Mg | C. | Cu | D. | Au |
15.LED系列产品是一类新型节能产品.图甲是NaBH4/H2O2燃料电池,图乙是LED发光二极管的装置示意图.下列叙述错误的是( )
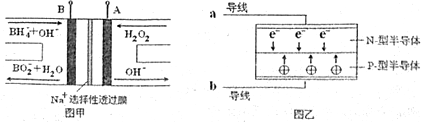

| A. | 电池A极区的电极反应式为:H2O2+2e-=2OH- | |
| B. | 电池放电过程中,Na+从负极区向正极区移动 | |
| C. | 每有1mol NaBH4参加反应转移电子数为4NA | |
| D. | 要使LED发光二极管正常发光,图乙中的导线a应与图甲中的B极相连 |
 从原子、分子水平上帮助我们认识物质构成的规律:以微粒之间不同的作用力为线索,研究不同类型物质的有关性质:从物质结构决定性质的视角预测物质的有关性质.
从原子、分子水平上帮助我们认识物质构成的规律:以微粒之间不同的作用力为线索,研究不同类型物质的有关性质:从物质结构决定性质的视角预测物质的有关性质. .
. 金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速.完成下列填空:
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速.完成下列填空: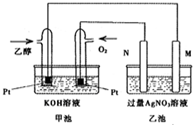 在298K时,1mol C2H5OH在氧气中完全燃烧生成二氧化碳和液态水放出热量1366.8kJ.
在298K时,1mol C2H5OH在氧气中完全燃烧生成二氧化碳和液态水放出热量1366.8kJ.