题目内容
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
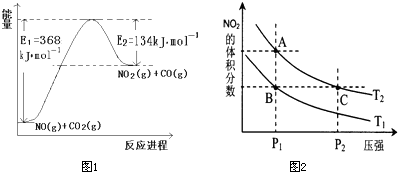
(1)下图是N2和H2反应生成2 mol NH3过程中能量变化示意图,请计算每生成1 mol NH3放出热量为________.

(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g),其化学平衡常数K与t的关系如下表:
2NH3(g),其化学平衡常数K与t的关系如下表:
请完成下列问题:
①试比较K1、K2的大小,K1________K2(填写“>”“=”或“<”)
![]()
②下列各项能作为判断该反应达到化学平衡状态的依据的是________(填序号字母).
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似.
①写出盐酸肼第一步水解反应的离子方程式________.
②盐酸肼水溶液中离子浓度的关系表示正确的是________(填序号).
A
.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)B.c(Cl-)>c([N2H5·H2O]+)>c(OH-)>c(H+)
C.2c(N2H62+)+c([N2H5·H2O]+)+c(H+)=c(Cl-)+c(OH-)
D.c(N2H62+)>c(Cl-)>c(H+)>c(OH-)
答案:
解析:
解析:
|
(1)46.1 kJ (2)> C (3)①N2H62++H2O ②AC |

练习册系列答案
相关题目
 氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.