��Ŀ����
7��A��B��C��D��E��FΪ�˵�������������Ҿ�С��18��ͬ����Ԫ�أ���֪A��C��F��ԭ�ӵ�������Ӳ㹲��11�����ӣ���������Ԫ�ص�����������Ӧ��ˮ����֮���������ܷ�Ӧ���������κ�ˮ��DԪ��ԭ�ӵ������������ȴ������4����EԪ��ԭ�Ӵ�����������������������3�����Իش���1��д��Ԫ�ط��ţ�ANa��DSi��EP��
��2���õ���ʽ��ʾB��F�γɻ�����Ĺ��̣�
 ��
����3��A��C��Ԫ�ص�����������Ӧˮ�������Ӧ�����ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O��
��4��D�Ĺ�̬������ΪSiO2����n mol D���������к�D-O���ۼ�Ϊ4nNA��
���� A��B��C��D��E��FΪ�˵�������������Ҿ�С��18��ͬ����Ԫ�أ�˵������Ԫ�ض�λ�ڶ����ڣ�DԪ��ԭ�ӵ������������ȴ������4������D����3�����Ӳ㣬����㺬��4�����ӣ�ΪSiԪ�أ�EԪ��ԭ�Ӵ�����������������������3������E����㺬��5�����ӣ�ΪPԪ�أ�A��C��F��ԭ�ӵ�������Ӳ㹲��11�����ӣ���������Ԫ�ص�����������Ӧ��ˮ����֮���������ܷ�Ӧ���������κ�ˮ����CΪAlԪ�أ�AΪNaԪ�أ�F������������=11-1-3-7����FΪClԪ�أ����ԭ��������С��֪BΪMgԪ�أ��ݴ˽��Ԫ��������֪ʶ���
��� �⣺A��B��C��D��E��FΪ�˵�������������Ҿ�С��18��ͬ����Ԫ�أ�˵������Ԫ�ض�λ�ڶ����ڣ�DԪ��ԭ�ӵ������������ȴ������4������D����3�����Ӳ㣬����㺬��4�����ӣ�ΪSiԪ�أ�EԪ��ԭ�Ӵ�����������������������3������E����㺬��5�����ӣ�ΪPԪ�أ�A��C��F��ԭ�ӵ�������Ӳ㹲��11�����ӣ���������Ԫ�ص�����������Ӧ��ˮ����֮���������ܷ�Ӧ���������κ�ˮ����CΪAlԪ�أ�AΪNaԪ�أ�F������������=11-1-3-7����FΪClԪ�أ����ԭ��������С��֪BΪMgԪ�أ�
��1�����ݷ�����֪��A��D��E�ֱ�ΪNa��Si��PԪ�أ�
�ʴ�Ϊ��Na��Si��P��
��2��B��F�γɻ�����Ϊ�Ȼ�þ���Ȼ�þΪ���ӻ�����õ���ʽ��ʾ���γɹ���Ϊ�� ��
��
�ʴ�Ϊ�� ��
��
��3��AΪNa��CΪAl�����ߵ�����������Ӧˮ����ֱ�Ϊ�������ơ��������������߷�Ӧ�����ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��4��DΪSiԪ�أ�Si�Ĺ�̬������ΪSiO2���������辧���У�1��O����2��Si��1��Si����4��O����1mol���������к���Si-O�������ʵ���Ϊ��1mol��[��2��2��$\frac{1}{2}$��+1��4��$\frac{1}{2}$]=4mol����n mol SiO2���������к�Si-O���ۼ������ʵ���Ϊ4nmol����ĿΪ4nNA��
�ʴ�Ϊ��SiO2��4n��
���� ���⿼����λ�ýṹ�����ʹ�ϵ���ۺ�Ӧ�ã���Ŀ�Ѷ��еȣ��ƶ�Ԫ��Ϊ���ؼ���ע������ԭ�ӽṹ��Ԫ�����ڱ���Ԫ�������ɵĹ�ϵ����4��Ϊ�״��㣬ע�����þ�̯��������������к��й�������Ŀ��

 ��ĩ100�ִ��غ�������ϵ�д�
��ĩ100�ִ��غ�������ϵ�д� Сѧ�������Ծ�ϵ�д�
Сѧ�������Ծ�ϵ�д�| A�� | a��b��e��c��d | B�� | b��e��a��d��c | C�� | a��e��b��c��d | D�� | a��d��b��e��c |
| �¶� | K |
| 973K | 1.47 |
| 1173K | 2.15 |
��2���÷�Ӧƽ�ⳣ���ı���ʽΪK=$\frac{C��CO��}{C��C{O}_{2}��}$��
| A�� | �������ʵ�����MgCl2��Ba��OH��2��HNO3������Һ��ϣ�Mg2++2OH-�TMg��OH��2�� | |
| B�� | CaCO3����CH3COOH��CaCO3+2H+�TCa2++CO2��+H2O | |
| C�� | ����HI��Һ���뵽Fe��NO3��3��Һ�У�2Fe3++2I-�T2Fe2++I2 | |
| D�� | ��NaClO��Һ��ͨ������SO2��3ClO-+SO2+H2O�T2HClO+SO42-+Cl- |
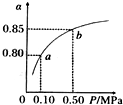 ��֪2A��g��+B��g��?2C��g�������ݻ�Ϊ1L���ܱ������м���0.50mol A��0.25mol B����500��ʱ��ַ�Ӧ����ƽ�����c��C��=0.4mol•L-1���ų�����Q1 kJ��
��֪2A��g��+B��g��?2C��g�������ݻ�Ϊ1L���ܱ������м���0.50mol A��0.25mol B����500��ʱ��ַ�Ӧ����ƽ�����c��C��=0.4mol•L-1���ų�����Q1 kJ��