题目内容
15.NA代表阿伏伽德罗常数的值,下列说法正确的是( )| A. | 7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.2×6.02×1023 | |
| B. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 0.1molNa2O2与足量二氧化碳充分反应转移的电子数为0.2NA | |
| D. | 0.1molFe在0.1mol氯气中燃烧,转移的电子数为0.2NA |
分析 A.氯气与氢氧化钠溶液的反应中,氯气既是氧化剂又是还原剂;
B.浓盐酸与二氧化锰的反应加入生成氯气,而稀盐酸不与氯气反应,浓盐酸变成稀盐酸后反应停止;
C.0.1mol过氧化钠与足量二氧化碳反应生成0.05mol氧气,结合过氧化钠中氧元素的化合价为-1价分析转移电子的物质的量及数目;
D.氯气不足,转移分子数按照氯气的物质的量计算.
解答 解:A.7.1g氯气的物质的量为:$\frac{7.1g}{71g/mol}$=0.1mol,0.1mol氯气与足量的氢氧化钠溶液反应时转移了0.1mol电子,转移的电子数为0.1×6.02×1023,故A错误;
B.50ml 12mol/L盐酸中含有0.6molHCl,由于稀盐酸不与二氧化锰反应,则反应生成的氯气小于0.15mol,反应转移电子的物质的量小于0.3mol,转移的电子数小于0.3NA,故B错误;
C.0.1molNa2O2与足量二氧化碳充分反应生成0.05mol氧气,转移了0.1mol电子,转移的电子数为0.1NA,故C错误;
D.0.1molFe在0.1mol氯气中燃烧,氯气不足,0.1mol氯气完全反应得到0.2mol电子,转移的电子数为0.2NA,故D正确;
故选D.
点评 本题考查阿伏加德罗常数,侧重考查氧化还原反应,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的分析能力及化学计算能力.

练习册系列答案
相关题目
6.下列物质的俗名与化学式相对应的是( )
| A. | 生石灰-Ca(OH)2 | B. | 石膏-Na2SO4•10H2O | ||
| C. | 水玻璃-Na2SiO3水溶液 | D. | 纯碱-NaOH |
3.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 在水溶液中:H+、I-、NO3-、SiO32- | |
| B. | 饱和氯水中:Cl-、NO3-、Na+、SO3- | |
| C. | 将足量CO2通入时:H+、NH4+、Al3+、SO42- | |
| D. | 加入金属铝产生H2的溶液中:NH4+、Na+、SO42-、CH3COO- |
10.“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义.请回答下列问题:
Ⅰ、石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成CaO•3MgO•4SiO2.
Ⅱ、某稻壳灰的成分为:
通过如图流程可由稻壳灰制备较纯净的二氧化硅.
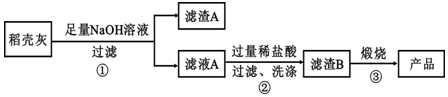
请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程式为SiO2+2OH-=SiO32-+H2O.
(3)滤渣A的成分有C和Fe2O3(填化学式)
(4)步骤②洗涤沉淀的方法是:往漏斗里的沉淀中注入蒸馏水致水浸没沉淀,让水自然流下,重复2-3次
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三角架.
Ⅰ、石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成CaO•3MgO•4SiO2.
Ⅱ、某稻壳灰的成分为:
| 组 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程式为SiO2+2OH-=SiO32-+H2O.
(3)滤渣A的成分有C和Fe2O3(填化学式)
(4)步骤②洗涤沉淀的方法是:往漏斗里的沉淀中注入蒸馏水致水浸没沉淀,让水自然流下,重复2-3次
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三角架.
20.下列事实不能证明CH3COOH是弱电解质的是( )
| A. | 0.1 moI/L的CH3COOH溶液的pH=2.1 | |
| B. | 等pH等体积的盐酸、CH3COOH溶液和足量锌反应,CH3COOH放出的氢气较多 | |
| C. | 用CH3COOH溶液做导电实验,灯泡很暗 | |
| D. | 0.1 moI/L的CH3COOH溶液稀释100倍,pH<3. |
7.氮化铝(AlN)是一种新型无机材料,广泛应用于电子、陶瓷等工业领域.在一定条件下,AlN可通过反应Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO合成.已知AlN可与NaOH溶液反应放出有刺激性气味的气体.下列叙述正确的是( )
| A. | AlN中氮元素的化合价为+3 | |
| B. | 上述反应中,N2是还原剂,Al2O3是氧化剂 | |
| C. | 上述反应中,每生成1molAlN需转移6mol电子 | |
| D. | AlN与NaOH溶液反应的化学方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑ |
4.下列关于漂白粉的叙述正确的是( )
| A. | 漂白粉的有效成分是Ca(ClO)2 | |
| B. | 漂白粉暴露在空气中久置不会变质 | |
| C. | 漂白粉是由Cl2与石灰乳制得 | |
| D. | 漂白粉变质过程中不涉及氧化还原反应 |