题目内容
现欲配制氢氧化铁胶体,将 逐滴滴入沸水中,继续煮沸至液体变为红褐色;用此分散系进行实验:
(1)将其装入U形管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色 ,这种现象称为 .
(2)向其中逐滴加入过量稀硫酸,现象是 .
(3)提纯此分散系的方法叫 .
(1)将其装入U形管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色
(2)向其中逐滴加入过量稀硫酸,现象是
(3)提纯此分散系的方法叫
考点:胶体的重要性质
专题:溶液和胶体专题
分析:将饱和的FeCl3溶液逐滴滴入沸水中,液体变为红褐色,得到的是Fe(OH)3胶体.发现阴极附近颜色逐渐变深,这表明Fe(OH)3胶粒带正电荷,另外胶体能聚沉,据此填空即可.
解答:
解:胶体制取方法是:将饱和的FeCl3溶液逐滴滴入沸水中,液体变为红褐色,得到的是Fe(OH)3胶体,故答案为:饱和三氯化铁溶液;
(1)阴极附近颜色逐渐变深,表明Fe(OH)3胶粒带正电荷,这种现象称为电泳,
故答案为:逐渐变深;电泳;
(2)稀硫酸数电解质,能使胶体出现聚沉现象,由于稀硫酸属于酸,故能溶解氢氧化铁沉淀,故答案为:先出现红褐色沉淀,后沉淀溶解;
(3)胶体粒子不能透过半透膜,提纯胶体的方法是渗析,故答案为:渗析.
(1)阴极附近颜色逐渐变深,表明Fe(OH)3胶粒带正电荷,这种现象称为电泳,
故答案为:逐渐变深;电泳;
(2)稀硫酸数电解质,能使胶体出现聚沉现象,由于稀硫酸属于酸,故能溶解氢氧化铁沉淀,故答案为:先出现红褐色沉淀,后沉淀溶解;
(3)胶体粒子不能透过半透膜,提纯胶体的方法是渗析,故答案为:渗析.
点评:本题考查胶体的性质,难度不大,掌握胶体的制备是解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、盐溶液都是中性的 |
| B、盐溶液的酸碱性与盐的类型无关 |
| C、碳酸钠溶液显碱性,是因为溶液中c(OH-)>c(H+) |
| D、NaHCO3溶液显酸性 |
下列关于原电池的叙述中,正确的是( )
| A、原电池中,正极就是阳极,负极就是阴极 |
| B、原电池工作时,在负极上发生氧化反应 |
| C、原电池工作时,溶液中的阳离子向负极移动 |
| D、电流从负极沿外电路流向正极 |
下列变化需要加入还原剂才能实现的是( )
| A、HCO3-→CO2 |
| B、MnO4-→Mn2+ |
| C、FeO→Fe3O4 |
| D、Zn→Zn2+ |
浓度为14%的KOH溶液加热蒸发掉100g水后变成28%的KOH溶液80mL,则后者溶液的浓度可能是( )
| A、6mol?L-1 |
| B、6.75mol?L-1 |
| C、6.25mol?L-1 |
| D、无法计算 |
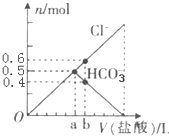 向某碳酸钠溶液中逐滴加1mol?L─1的盐酸,测得溶液中Cl-、HCO3-的物质的量随加入盐酸体积的关系如图所示,则下列说法中正确的是( )
向某碳酸钠溶液中逐滴加1mol?L─1的盐酸,测得溶液中Cl-、HCO3-的物质的量随加入盐酸体积的关系如图所示,则下列说法中正确的是( )| A、Oa段反应的离子方程式与ab段反应的离子方程式相同 |
| B、该碳酸钠溶液中含有1mol Na2CO3 |
| C、b点的数值为0.6 |
| D、b点时生成CO2的物质的量为0.3 mol |
与9.6g SO2所含的氧原子数相等的NO2的质量为( )
| A、9.6g | B、6.9g |
| C、4.6g | D、2.3g |