题目内容
19.下列关于元素周期表的说法,错误的是( )| A. | 元素周期表是元素按原子量大小排列而成的 | |
| B. | 从第一周期到第三周期元素,其原子的价电子数和族数是一致的 | |
| C. | 主族元素中(氢除外)族序数越小的元素,其最高价氧化物的水化物碱性越强 | |
| D. | 元素周期表是元素周期律的具体表现形式 |
分析 A.元素周期表是按原子序数大小排列的,不是按原子量大小排列;
B.短周期元素中,原子的价电子数和族数是一致;
C.同一主族中,原子序数越大,最高价氧化物对应水合物的碱性越强;
D.元素周期律是核外电子周期性变化的必然结果.
解答 解:A.元素周期表中原子序数为周期性变化,则元素周期表是元素按原子序数大小排列而成的,故A错误;
B.从第一周期到第三周期元素为短周期元素,各原子的价电子数和族数是一致的,故B正确;
C.主族元素中(氢除外)族序数越小的元素,金属性越弱,其最高价氧化物的水化物碱性越强,故C正确;
D.元素周期律是核外电子周期性变化的必然结果,则元素周期表是元素周期律的具体表现形式,故D正确;
故选A.
点评 本题考查元素周期表结构及应用,题目难度不大,熟悉元素在周期表中的位置及元素的性质即可解答,注重元素位置与性质的考查.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列实验操作与实验目的相对应的是( )
| 实验操作 | 实验目的 | |
| A | 制乙炔时用饱和食盐水代替水 | 加快化学反应速率 |
| B | C2H4与SO2混合气体通过盛有溴水的洗气瓶 | 除去C2H4中的SO2 |
| C | 淀粉溶液水解后冷却至室温,加碘水观察现象 | 检验淀粉是否完全水解 |
| D | 将溴乙烷与氢氧化钠水溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验溴乙烷中的溴原子 |
| A. | A | B. | B | C. | C | D. | D |
13.甲、乙两容器中都在进行A?B+C的反应,甲中每分钟减少4mol A,乙中每分钟减少2mol A,则甲、乙两容器中的反应速率的比较是( )
| A. | 甲快 | B. | 乙快 | C. | 相等 | D. | 无法确定 |
4.一种浓硫酸溶液的浓度为amol•L-1,密度为ρ g•cm3,则这种溶液中,溶质的质量分数是( )
| A. | $\frac{1000a}{98ρ}$×100% | B. | $\frac{98ρ}{1000a}$×100% | C. | $\frac{1000ρ}{98a}$×100% | D. | $\frac{98a}{1000ρ}$×100% |
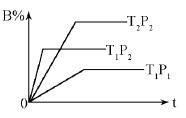
 pC(g) △H=Q kJ·mol-1,在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是
pC(g) △H=Q kJ·mol-1,在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是