题目内容
已知某可逆反应:mA(g)+nB(g)  pC(g) △H=Q kJ·mol-1,在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是
pC(g) △H=Q kJ·mol-1,在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是
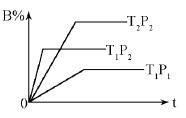
A.T1<T2 P1>P2 m+n>p ΔΗ<0
B.T1>T2 P1<P2 m+n<p ΔΗ>0
C.T1<T2 P1>P2 m+n<p ΔΗ<0
D.T1 >T2 P1<P2 m+n>p ΔΗ>0
练习册系列答案
相关题目
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 28g N2所含的原子数目为NA | |
| B. | 标准状况下,18 g H2O所占的体积约为22.4 L | |
| C. | 0.5 mol H2SO4含有的原子数目为3.5NA | |
| D. | 在常温常压下,11.2 L N2含有的原子数为NA |
19.下列关于元素周期表的说法,错误的是( )
| A. | 元素周期表是元素按原子量大小排列而成的 | |
| B. | 从第一周期到第三周期元素,其原子的价电子数和族数是一致的 | |
| C. | 主族元素中(氢除外)族序数越小的元素,其最高价氧化物的水化物碱性越强 | |
| D. | 元素周期表是元素周期律的具体表现形式 |
16.把100g某NaOH溶液(密度是1.2g.mL-1)蒸发浓缩,余下50mL溶液时,物质的量浓度为8mol•L-1,原溶液的浓度是( )
| A. | 8mol•L-1 | B. | 4.8mol•L-1 | C. | 3.3mol•L-1 | D. | 16mol•L-1 |
4.常温下,向1L0.1mol/L H2A溶液中逐滴加入等浓度NaOH溶液,所得溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图所示,则下列说法中正确的是( )
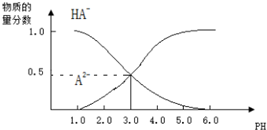

| A. | H2A的电离方程式为:H2A?H++HA-,HA-?H++A2- | |
| B. | 0.1mol/LNaHA溶液中存在c(A2-)+c(HA-)+c(H2A)=0.1mol/L | |
| C. | 常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0 | |
| D. | pH=4.0时,图中n(HA-)约为0.0091mol |