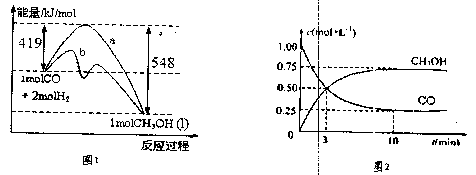题目内容
反应CO(g)+2H2(g)?2CH3OH(g)在密闭容器中进行.为探究温度、CO2等对该反应的影响,进行了4组实验,结果如图.下列说法不正确的是( )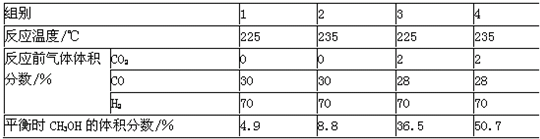

| A、该反应的△H>0 | B、当容器中压强不变时,反应达到平衡 | C、CH3OH含量增大的原因是CO2起了催化作用 | D、少量CO2能提高平衡时CH3OH的体积分数 |
分析:A、比较表中1和2或者3和4数据可知,其他条件一致时,升高温度,达到平衡时CH3OH体积分数增大,判断△H;
B.反应前气体体积大于反应后气体体积,即化学平衡移动时,压强也随之变化,据此判断;
C.有CO2存在时,能促进反应的正向移动,但不是催化作用;
D.比较表中1和3或者2和4数据可知,CO2存在,能够增大CH3OH的体积分数.
B.反应前气体体积大于反应后气体体积,即化学平衡移动时,压强也随之变化,据此判断;
C.有CO2存在时,能促进反应的正向移动,但不是催化作用;
D.比较表中1和3或者2和4数据可知,CO2存在,能够增大CH3OH的体积分数.
解答:解:A、比较表中1和2或者3和4数据可知,其他条件一致时,升高温度,化学平衡向着吸热的方向移动,达到平衡时CH3OH体积分数增大,所以△H>0,故A正确;
B.反应前气体体积大于反应后气体体积,即化学平衡移动时,压强也随之变化,当压强不变时,达到了化学平衡状态,故B正确;
C.有CO2存在时,能促进反应的正向移动,但不是催化作用,催化作用不影响化学平衡的移动,只影响化学反应速率,故C错误;
D.比较表中1和3或者2和4数据可知,CO2存在,能够增大CH3OH的体积分数,故D正确;
故选C.
B.反应前气体体积大于反应后气体体积,即化学平衡移动时,压强也随之变化,当压强不变时,达到了化学平衡状态,故B正确;
C.有CO2存在时,能促进反应的正向移动,但不是催化作用,催化作用不影响化学平衡的移动,只影响化学反应速率,故C错误;
D.比较表中1和3或者2和4数据可知,CO2存在,能够增大CH3OH的体积分数,故D正确;
故选C.
点评:本题考查化学平衡移动的影响因素,根据表中数据比较得到答案,难度不大.

练习册系列答案
相关题目
 CH3OH
CH3OH
 CH3OH(g)的平衡常数为 ;10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。
CH3OH(g)的平衡常数为 ;10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。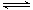 CH3OH
CH3OH
 CH3OH(g)的平衡常数为 ;10min后,容器内的压强变为原来的
倍;改变下列条件,能提高CO转化率的是
。
CH3OH(g)的平衡常数为 ;10min后,容器内的压强变为原来的
倍;改变下列条件,能提高CO转化率的是
。