��Ŀ����
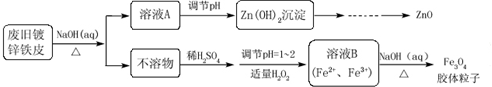
20������һ����Ҫ����������������Ҫ�ɷ�ΪAl2O3��Fe2O3��SiO2�ȣ���ұ��Al�Ĺ�ҵ������������ͼ��
��1������B�Ļ�ѧʽΪSiO2����ҺA�к�����������Ҫ��Al3+��Fe3+��H+��
��2��д������II������ҺC �����ӷ���ʽAl3++4OH-=[Al��OH��4]-������I����Ҫ�õ��ķ��뷽���ǹ��ˣ�
��3�����������У���CaO����ѭ��ʹ���⣬������ѭ��ʹ�õ������У�CO2��NaOH���ѧʽ����
��4���������������ȷ�Ӧ���Ӹֹ죬������������������Ӧ�Ļ�ѧ����ʽΪ��2Al+Fe 2O3 $\frac{\underline{\;����\;}}{\;}$Al 2O3 +2Fe
��5����������a�����������ұ����b�ֵ������������������������ģ�����ԭ��������Al2O3�Ĵ��ȣ�����������$\frac{17b}{9a}$��100%���ú�a��b�����ʽ��ʾ����
���� �ɹ������̿�֪����������Ҫ�ɷ�ΪAl2O3��Fe2O3��SiO2�ȣ�������������������ᷴӦ�ó���B����ҺA�������BΪSiO2�����˵���ҺA�����Ȼ������Ȼ���������ȣ���Һ�м��������NaOH������֪����DΪ�������������˵���ҺC����ƫ�����ơ��Ȼ��ƣ���������ҺC��ͨ�������̼����������������������ҺEΪ̼�����ƻ�̼������Һ�����˺���E��Һ�м��������Ƶó���GΪ̼��ƣ�ͬʱ�õ�����������Һ������������Һ����ѭ�����ã�̼������շֽ�������ƺͶ�����̼������ѭ�����ã�Al��OH��3���յ���������������ڵ��������ɵ������ݴ˴��⣻
��� �⣺�ɹ������̿�֪����������Ҫ�ɷ�ΪAl2O3��Fe2O3��SiO2�ȣ�������������������ᷴӦ�ó���B����ҺA�������BΪSiO2�����˵���ҺA�����Ȼ������Ȼ���������ȣ���Һ�м��������NaOH������֪����DΪ�������������˵���ҺC����ƫ�����ơ��Ȼ��ƣ���������ҺC��ͨ�������̼����������������������ҺEΪ̼�����ƻ�̼������Һ�����˺���E��Һ�м��������Ƶó���GΪ̼��ƣ�ͬʱ�õ�����������Һ������������Һ����ѭ�����ã�̼������շֽ�������ƺͶ�����̼������ѭ�����ã�Al��OH��3���յ���������������ڵ��������ɵ�����
��1����������ķ�����֪������B�Ļ�ѧʽΪSiO2����ҺA�к�����������Ҫ�� Al3+��Fe3+��H+��
�ʴ�Ϊ��SiO2�� Al3+��Fe3+��H+��
��2������II�����������������Ȼ�����Ӧ����ƫ�����ƣ���Ӧ�����ӷ���ʽ ΪAl3++4OH-=[Al��OH��4]-����������ķ�����֪������I����Ҫ�õ��ķ��뷽���� ���ˣ�
�ʴ�Ϊ��Al3++4OH-=[Al��OH��4]-�����ˣ�
��3�����������У���CaO����ѭ��ʹ���⣬������ѭ��ʹ�õ�������CO2��NaOH��
�ʴ�Ϊ��CO2��NaOH��
��4������������������Ӧ�Ļ�ѧ����ʽΪ��2Al+Fe 2O3 $\frac{\underline{\;����\;}}{\;}$Al 2O3 +2Fe��
�ʴ�Ϊ��2Al+Fe 2O3 $\frac{\underline{\;����\;}}{\;}$Al 2O3 +2Fe��
��5��a�����������ұ����b�ֵ������������Ԫ���غ��֪����Ҫ��������������Ϊ$\frac{102}{54}$b�֣�����ԭ��������Al2O3�Ĵ���Ϊ$\frac{\frac{102}{54}b}{a}$��100%=$\frac{17b}{9a}$��100%��
�ʴ�Ϊ��$\frac{17b}{9a}$��100%��
���� ������ұ������ȡ��������Ϊ���忼���������ʵ�鷽������ƣ�Ϊ��Ƶ���㣬�漰�����ƶϡ�Ԫ�ػ��������ʼ��ת�������ӵķ��������ӷ���ʽ����ѧ����ȣ����ط�����ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ�

 ����������ϵ�д�
����������ϵ�д�| A�� | ��﮺Ͻ���������γɵ�һ�ֻ����� | |
| B�� | ��Ǽ����Ԫ�أ����ʻ��ã���﮺Ͻ���ˮ��Ӧ�������� | |
| C�� | �����Ӻ�����ӵĺ�������Ų���ͬ | |
| D�� | ����﮺Ͻ���﮺���Ϊ1.1%����127.3g��﮺Ͻ��к����ԭ��0.2mol |
| A�� | NaNO3 | B�� | NO2 | C�� | NO | D�� | N2 |