题目内容
20.常温下,将12.5g CuSO4•5H2O溶解于47.5g水中形成CuSO4溶液,设该溶液密度为1.20g/cm3,求:(1)该溶液中CuSO4的物质的量;
(2)该溶液中CuSO4的物质的量浓度;
(3)取出20.0mL该溶液,配成0.50mol/L的稀溶液,则稀释后溶液的体积是多少?
分析 (1)根据n=$\frac{m}{M}$计算 CuSO4•5H2O的物质的量,溶液中n(CuSO4)=n( CuSO4•5H2O);
(2)根据V=$\frac{m}{ρ}$计算溶液体积,再根据c=$\frac{m}{V}$计算溶液中CuSO4的物质的量浓度;
(3)根据稀释定律C浓V浓=C稀V稀计算稀释后溶液体积.
解答 解:(1)溶液中n(CuSO4)=n( CuSO4•5H2O)=$\frac{12.5g}{250g/mol}$=0.05mol,
答:溶液中CuSO4的物质的量为0.05mol;
(2)溶液的体积V=$\frac{12.5g+47.5g}{1200g/L}$=0.05L,则溶液中CuSO4的物质的量浓度为$\frac{0.05mol}{0.05L}$=1mol/L,
答:溶液中CuSO4的物质的量浓度为1mol/L;
(3)设稀释后溶液的体积是VL,根据稀释定律C浓V浓=C稀V稀可知:
1mol/L×0.02L=0.5mol/L×VL
解得:V=0.04L=40mL,
答:稀释后溶液的体积是40mL.
点评 本题考查物质的量浓度的计算,注意对公式的理解与灵活应用,难度不大.

练习册系列答案
相关题目
2.已知某无色溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是( )
| A. | CO32-、Cl- | B. | Na+、Cu2+ | C. | Mg2+、C1- | D. | C1-、Ba2+ |
10.工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2.在该反应中( )
| A. | 硫元素既被氧化又被还原 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 每生成1molNa2S2O3,转移4mol电子 | |
| D. | 当转移8mol电子时,还原产物比氧化产物多1mol |
15.进行化学实验时应强化安全意识,下列做法正确的是( )
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| C. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 | |
| D. | 少量金属汞洒落在实验室地面或桌面时,应立即向汞上撒硫黄粉,然后再清扫 |
9.正确的实验操作是实验成功的重要因素,下列实验操作正确的是( )
| A. | 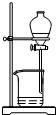 放出碘的苯溶液 放出碘的苯溶液 | B. | 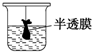 分离或提纯胶体 分离或提纯胶体 | ||
| C. | 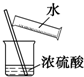 实验室稀释浓硫酸 实验室稀释浓硫酸 | D. | 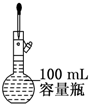 定容 定容 |
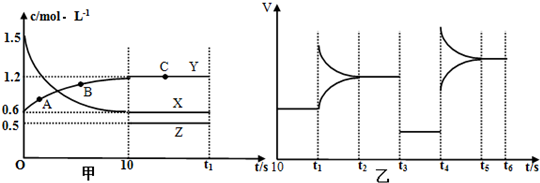
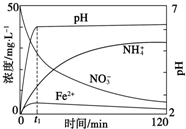 工、农业废水及生活污水中浓度较高的NO${\;}_{3}^{-}$会造成氮污染,工业上处理水体中NO${\;}_{3}^{-}$的一种方法是单质铁化学还原法.某化学小组用废铁屑和硝酸盐溶液模拟此过程,实验如下.
工、农业废水及生活污水中浓度较高的NO${\;}_{3}^{-}$会造成氮污染,工业上处理水体中NO${\;}_{3}^{-}$的一种方法是单质铁化学还原法.某化学小组用废铁屑和硝酸盐溶液模拟此过程,实验如下.