题目内容
10.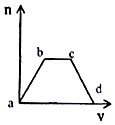 将足量CO2通入KOH和Ca(OH)2的混合溶液中,生成沉淀的质量(m)和通入CO2体积(V)的关系如图所示:
将足量CO2通入KOH和Ca(OH)2的混合溶液中,生成沉淀的质量(m)和通入CO2体积(V)的关系如图所示:(1)ab段发生的离子反应方程式为CO2+2OH-+Ca2+=CaCO3↓+H2O.
(2)bc段依次发生两个离子反应,首先是CO2+2OH-=CO32-+H2O,其次是CO2+CO32-+H2O=2HCO3-.
(3)cd段发生的离子反应方程式是CO2+H2O+CaCO3=Ca2++2HCO3-.
分析 向KOH和Ca(OH)2的混合稀溶液中通入CO2,氢氧化钙优先反应(ab段),反应的方程式为CO2+Ca(OH)2=CaCO3↓+H2O;然后KOH与二氧化碳反应(bc段):2KOH+CO2═K2CO3、K2CO3+H2O+CO2═2KHCO3;最后碳酸钙沉淀溶解(cd):CaCO3+H2O+CO2═Ca(HCO3)2,据此书写反应的离子方程式.
解答 解:(1)ab段氢氧化钙优先与二氧化碳反应生成碳酸钙沉淀和水,反应的离子方程式为:CO2+2OH-+Ca2+=CaCO3↓+H2O,
故答案为:CO2+2OH-+Ca2+=CaCO3↓+H2O;
(2)bc段KOH与二氧化碳反应生成碳酸钾,碳酸钾与二氧化碳反应生成碳酸氢钾,反应的离子方程式为:CO2+2OH-=CO32-+H2O、CO2+CO32-+H2O=2HCO3-,
故答案为:CO2+2OH-=CO32-+H2O;CO2+CO32-+H2O=2HCO3-;
(3)cd段沉淀逐渐减少,说明碳酸钙与二氧化碳反应生成碳酸氢钙,反应的离子方程式为:CO2+H2O+CaCO3=Ca2++2HCO3-,
故答案为:CO2+H2O+CaCO3=Ca2++2HCO3-.
点评 本题考查了离子方程式的书写,题目难度中等,明确发生反应的先后顺序为解答关键,注意掌握离子方程式的书写原则是,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
18.下列既是吸热反应,又是氧化还原反应的是( )
| A. | 碳在高温下和二氧化碳的反应 | B. | 碳不完全燃烧 | ||
| C. | 氯化铵与氢氧化钡晶体的反应 | D. | 铝和氧化铁在高温下的反应 |
5.下列物质必须隔绝空气密封保存的是( )
①Na ②镁条 ③石灰水④NaOH ⑤Na2CO3•10H2O ⑥NaCl.
①Na ②镁条 ③石灰水④NaOH ⑤Na2CO3•10H2O ⑥NaCl.
| A. | ①② | B. | ①③④⑤ | C. | ①②③④ | D. | ①②①②④⑤ |
15.下列各组离子在溶液中能大量共存的是( )
| A. | Na+、Mg2+、Cl-、SO42- | B. | Cu2+、Cl-、NO3-、OH- | ||
| C. | Ca2+、Na+、CO32-、NO3- | D. | K+、Fe3+、NO3-、SCN- |
