题目内容
5.汽车尾气中的CO、NO都是城市空气中浓度较高、危害严重的污染物,下列有关它们的叙述中不正确的是( )| A. | CO、NO均难溶于水 | |
| B. | CO、NO均为酸性氧化物 | |
| C. | CO、NO均为无色无味的有毒气体 | |
| D. | 在催化剂的作用下,可通过反应2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2来达到净化汽车尾气的目的 |
分析 CO和NO都难溶于水的无色无味的气体,二者都不能与碱溶液反应,都不与酸性氧化物;通过反应2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2可达到净化汽车尾气的目的,据此进行解答.
解答 解:A.CO、NO都是难溶于水的气体,故A正确;
B.CO、NO都不与碱反应,都不是酸性氧化物,故B错误;
C.CO、NO均为无色无味、有毒的气体,故C正确;
D.在催化剂的作用下,反应2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2将有毒气体转化成无毒的氮气和二氧化碳,从而达到净化汽车尾气目的,故D正确;
故选B.
点评 本题考查了常见气体的性质及应用,题目难度不大,明确一氧化碳、一氧化氮的性质为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
16.下列说法正确的是( )
| A. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液变红 | |
| B. | 只存在共价键的物质一定是共价化台物、离子化合物中一定含有离子键 | |
| C. | Na2O与Na2O2组成元素相同、阴阳离子个数比相同,但跟水反应的产物不同 | |
| D. | 元素原子的最外层电子数越多,得电子能力越强,失电子能力越弱 |
13.下列化学反应的离子方程式正确的是( )
| A. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| B. | 在稀氨水中通入少量CO2:2NH3•H2O+CO2═2NH4++CO32-+H2O | |
| C. | 用稀HCl溶液溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | Cl2与水反应:Cl2+H2O═HCl+HClO |
10.原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关.已知常温下,有下列3个装置.下列说法中正确的是( )
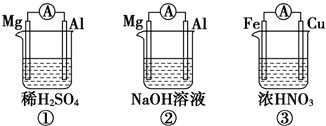

| A. | ①②中Mg作负极,③中Fe作负极 | |
| B. | ②中Al作正极,其电极反应式为Al-3e-=Al3+ | |
| C. | ③中Fe作负极,电极反应式为Fe-2e-=Fe2+ | |
| D. | 若①②中转移的电子数相同,则①②中产生的H2的量也一定相同 |
14.下列解释事实的离子方程式正确的是( )
| A. | 澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O | |
| B. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═Al(OH)4-+4NH4+ | |
| C. | 少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O═2C6H5OH+CO32- | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O |
 ;
;
 .
.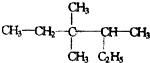 3,3,4-三甲基己烷
3,3,4-三甲基己烷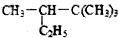 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷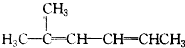 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯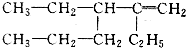 2,3-二乙基-1-己烯.
2,3-二乙基-1-己烯.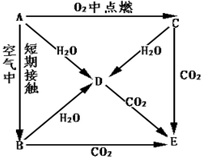 A、B、C、D、E五种物质的焰色反应均为黄色,且A为单质,它们按图所示关系相互转化.
A、B、C、D、E五种物质的焰色反应均为黄色,且A为单质,它们按图所示关系相互转化.