题目内容
8.以化合物A为原料合成化合物M的线路如图所示: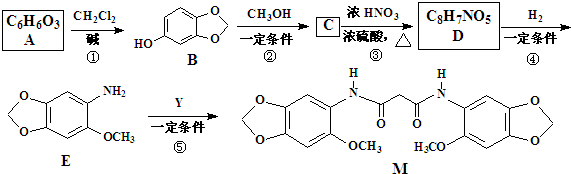
已知:
(Ⅰ)

(Ⅱ)
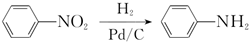
(1)写出下列反应的反应类型:反应①:取代反应;反应④:还原反应.
(2)有同学认为可以将②③两个反应调换位置,你认为是否可行?否(填“是”或“否”);并解释原因若先硝化,B中酚羟基容易被硝酸氧化,使M产率降低.
(3)写出化合物B中官能团的名称:(酚)羟基和醚键.
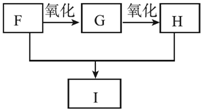
(4)若1 mol M在酸性条件下完全水解,理论上能生成2 mol W和1 mol N,N的结构简式为HOOCCH2COOH.已知N的同系物中含碳量最低的物质H和一些有机物间存在如图的转化关系,I为一种六元环状化合物,写出由F和H反应生成I的化学方程式
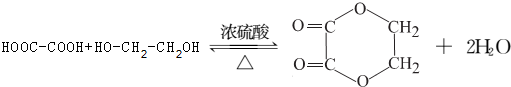 .
.
(5)F和H间也可以发生反应生成一种高分子化合物,写出该反应的化学方程式nHOOCCOOH+nHOCH2CH2OH$?_{△}^{浓硫酸}$
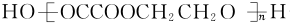 +(2n-1)H2O.
+(2n-1)H2O.
分析 由信息(Ⅰ)及反应①可推知A为 ,反应③是引入-NO2的反应,由信息(Ⅱ)可知反应④是-NO2被还原成-NH2的反应,E中的-OCH3应是反应②生成的,所以C是
,反应③是引入-NO2的反应,由信息(Ⅱ)可知反应④是-NO2被还原成-NH2的反应,E中的-OCH3应是反应②生成的,所以C是 ,D为
,D为 .
.
(4)M在酸性条件下水解生成的物质N应该是HOOCCH2COOH,其同系物中含碳量最低的是HOOCCOOH,根据信息,F为乙二醇,G为乙二醛,I为一种六元环状化合物,则I为 .
.
解答 解:由信息(Ⅰ)及反应①可推知A为 ,反应③是引入-NO2的反应,由信息(Ⅱ)可知反应④是-NO2被还原成-NH2的反应,E中的-OCH3应是反应②生成的,所以C是
,反应③是引入-NO2的反应,由信息(Ⅱ)可知反应④是-NO2被还原成-NH2的反应,E中的-OCH3应是反应②生成的,所以C是 ,D为
,D为 .
.
(1)除反应④是还原反应外,其余反应都是取代反应,
故答案为:取代反应;还原反应;
(2)若先硝化,B中酚羟基容易被硝酸氧化,使M产率降低,所以反应②③位置不能调换,
故答案为:否,若先硝化,B中酚羟基容易被硝酸氧化,使M产率降低;
(3)B中官能团为(酚)羟基和醚键,
故答案为:(酚)羟基和醚键;
(4)M在酸性条件下水解生成的物质N应该是HOOCCH2COOH,其同系物中含碳量最低的是HOOCCOOH,根据信息,F为乙二醇,G为乙二醛,I为一种六元环状化合物,则I为 .F和H反应生成I的化学方程式:
.F和H反应生成I的化学方程式: ,
,
故答案为:HOOCCH2COOH; ;
;
(5)F和H发生缩聚反应生成一种高分子化合物,该反应的化学方程式:nHOOCCOOH+nHOCH2CH2OH$?_{△}^{浓硫酸}$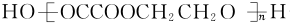 +(2n-1)H2O,
+(2n-1)H2O,
故答案为:nHOOCCOOH+nHOCH2CH2OH$?_{△}^{浓硫酸}$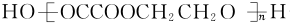 +(2n-1)H2O.
+(2n-1)H2O.
点评 本题考查有机物的推断、化学反应类型、官能团、同分异构体的书写、化工生产条件的控制等,注意根据有机物的结构与分子式进行分析解答,侧重考查学生的分析推理能力、知识迁移运用能力.

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案 实验室以2一丁醇(
实验室以2一丁醇( )为原料制备2-氯丁烷
)为原料制备2-氯丁烷(
 ),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:| 物质 | 熔点 (℃) | 沸点(℃) |
| 2-丁醇 | -114.7 | 99.5 |
| 2-氯乙烷 | -131.3 | 68.2 |
步骤1:在圆底烧瓶内放入无水ZnC12和12mol.L一1浓盐酸,充分溶解、冷却,再加入2一丁
醇,加热一段时间.
步骤2:将反应混合物移至蒸馏装置内,蒸馏并收集115℃以下馏分.
步骤3:从馏分中分离出有机相,依次用蒸馏水、5%NaoH溶液、蒸馏水
洗涤,再加入CaCl2固体,放置一段时间后过滤.
步骤4:滤液经进一步精制得产品
(1)加入烧瓶的物质中,有一种是催化剂,该物质是无水ZnCl2.
(2)反应装置中冷凝管的作用是冷凝回流提高原料利用率,烧杯内所盛液体可以是水或碱液.
(3)用NaoH溶液洗涤时操作要迅速,其原因是防止2-氯丁烷水解减少2-氯丁烷挥发,第二次用蒸馏水
洗涤的目的是除去残留的氢氧化钠.
(4)步骤4精制过程中不需使用的仪器是ad.
a.布氏漏斗b.抽滤瓶c.蒸馏烧瓶d.冷凝管.
| A. | 5.05×10-4mol/L | B. | 5.26×10-4mol/L | C. | 5.05×10-3mol/L | D. | 5.26×10-3mol/L |
| A. | 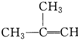 -CH3+Br2→ -CH3+Br2→ | |
| B. | CH2=CH-CH3+HCl→ | |
| C. | CH2=CH-CH=CH2+Br2→ | |
| D. | CH3-CH=CH2+H2O$→_{加热、加压}^{催化剂}$ |
| A. |  分子中至少有9个碳原子处于同一平面上 分子中至少有9个碳原子处于同一平面上 | |
| B. |  的核磁共振氢谱有5个峰 的核磁共振氢谱有5个峰 | |
| C. | 某烯烃与氢气加成后得到2,2-二甲基丁烷,该烯烃的名称是3,3-二甲基-1-丁烯 | |
| D. | 能够测定分子化学键的方法是核磁共振谱 |
| A. | Fe2+不能与SCN-形成血红色化合物 | B. | 该晶体中一定含有SCN- | ||
| C. | Fe3+的氧化性比氯气的氧化性强 | D. | Fe2+被氯气氧化成Fe3+ |
| A. | 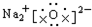 | B. | 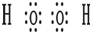 | ||
| C. | 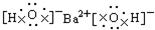 | D. | 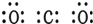 |
 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应: