题目内容
3.向一定体积的BaCl2溶液中加入V mL的0.01mol/L H2SO4溶液,两者恰好完全反应,且反应后溶液的PH是3.0,原BaCl2溶液物质的量浓度是( )| A. | 5.05×10-4mol/L | B. | 5.26×10-4mol/L | C. | 5.05×10-3mol/L | D. | 5.26×10-3mol/L |
分析 0.01mol/L硫酸溶液中c(H+)=0.02mol/L,硫酸与氯化钡发生反应Ba2++SO42-=BaSO4↓,反应后溶液的pH为3.0,则c(H+)=1×10-3mol/L,说明反应后硫酸体积为原溶液体积的20倍,以此解答该题.
解答 解:氯化钡与硫酸反应生成硫酸钡与HCl,反应中氢离子的物质的量不变,设氯化钡溶液的体积为xmL,利用氢离子物质的量列方程,则:
0.001mol/L×(V+x)mL=VmL×0.01mol/L×2,
解得:x=19V,
氯化钡与硫酸反应生成硫酸钡与HCl,氯化钡的物质的量等于硫酸的物质的量,色号氯化钡的浓度为ymol/L,
则:ymol/L×19VmL=0.01mol/L×VmL,
解得:y=5.26×10-4mol/L,
故选B.
点评 本题考查物质的量浓度有关计算、离子方程式的计算,为高频考点,题目难度中等,侧重于学生的分析能力和计算能力的考查,明确发生反应的实质为解答关键.

练习册系列答案
相关题目
13.下列各项表述与示意图一致的是( )


| A. | 图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0;使用和未使用催化剂时,反应过程中的能量变化 | |
| B. | 图②表示25℃时,用0.01mol•L-1盐酸滴定一定体积的0.01mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. | 图③表示CH4(g)+H2O(g)?CO(g)+3H2(g)△H,反应CH4的转化率与温度、压强的关系,且P1>P2、△H>0 | |
| D. | 图④中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0;正、逆反应的平衡常数K随温度的变化 |
14.下列氯的化合物中,不能由氯气与相应的金属反应制取的是( )
| A. | FeCl3 | B. | CuCl2 | C. | FeCl2 | D. | NaCl |
11.对下列化学用语或化学原理的理解和描述均正确的是( )
| A. | 电子式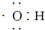 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 | |
| B. | 比例模型 可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 | |
| C. | 明矾能水解生成Al(OH)3胶体,可用作饮用水杀菌 | |
| D. | 原子结构示意图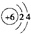 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C |
15.某烃经催化加氢后得到2-甲基丁烷,该烃不可能是( )
| A. | 2-甲基-2-丁烯 | B. | 3-甲基-1-丁烯 | C. | 3-甲基-2-丁烯 | D. | 2-甲基-1-丁烯 |
12.下列排序不正确的是( )
| A. | 气态氢化物稳定性 H2O<NH3<CH4 | B. | 微粒半径 Al3+<F-<Cl- | ||
| C. | 碱性 Mg(OH)2<NaOH<KOH | D. | 熔点 冰醋酸<食盐<金刚石 |
13.下列贮存化学试剂的方法正确的是( )
| A. | 浓硝酸保存在棕色的广口瓶中,并放在阴凉处 | |
| B. | 少量的金属钠应保存在煤油中 | |
| C. | 烧碱溶液放在带玻璃塞的磨口试剂瓶中 | |
| D. | 用做感光材料的溴化银贮存在无色试剂瓶中 |

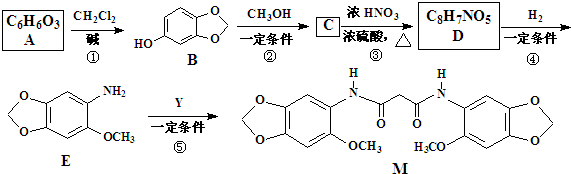

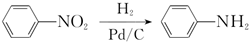
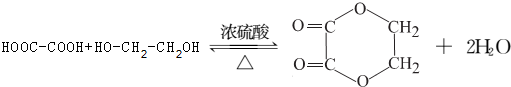 .
.
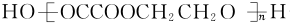 +(2n-1)H2O.
+(2n-1)H2O.