题目内容
常温下,在下列给定条件的溶液中,一定能大量共存的离子组是
A.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3—
B.加入铝粉生成H2的溶液:K+、Mg2+、SO42—、HCO3—
C.c(Fe3+)=0.1mol·L-1的溶液:H+、Al3+、I-、SCN-
D. =0.1mol·L-1的溶液:Na+、K+、SiO32—、NO3—
=0.1mol·L-1的溶液:Na+、K+、SiO32—、NO3—
D
【解析】
试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A.能使pH试纸呈红色的溶液显酸性,在酸性条件下I-、NO3—发生氧化还原反应,不能大量共存,A错误;B.加入铝粉生成H2的溶液可能显酸性,也可能显碱性,显酸性HCO3—不能大量共存。显碱性Mg2+、HCO3—均不能大量共存,B错误;C.c(Fe3+)=0.1mol·L-1的溶液I-、SCN-均不能大量共存,C错误;D.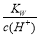 =0.1mol·L-1的溶液中氢氧根的浓度是0.1mol/L,溶液显碱性,则Na+、K+、SiO32—、NO3—均可以大量共存,D正确,答案选D。
=0.1mol·L-1的溶液中氢氧根的浓度是0.1mol/L,溶液显碱性,则Na+、K+、SiO32—、NO3—均可以大量共存,D正确,答案选D。
考点:考查离子共存的正误判断

练习册系列答案
相关题目
根据表中信息判断,下列选项不正确的是
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO | Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO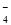 >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2

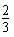 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)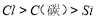
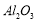 在工业上用于制作耐高温材料,也用于电解法治炼铝
在工业上用于制作耐高温材料,也用于电解法治炼铝