题目内容
18.前四周期元素X、Y、Z、W核电荷数依次增加,核电荷数之和为58;Y 原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2.(1)Z元素位于周期表第三周期第ⅦA族.
(2)Y与X形成共价化合物中Y的杂化方式是sp3,分子构型为三角锥形.
(3)Z的最高价氧化物的水化物的化学式为HClO4.
(4)W基态原子价电子排布图为
 ,W的最高正价为+7.
,W的最高正价为+7.
分析 前四周期元素X、Y、Z、W核电荷数依次增加,Y 原子的M层p轨道有3个未成对电子,则外围电子排布为3s23p3,故Y为P元素;Z与Y同周期,且在该周期中电负性最大,则Z为Cl元素;W原子的L层电子数与最外层电子数之比为4:1,最外层电子数为2,其d轨道中的电子数与最外层电子数之比为5:2,d轨道电子数目为5,外围电子排布为3d54s2,故W为Mn元素,而X、Y、Z、W四种元素的核电荷数之和为58,则X核电荷数为58-15-17-25=1,故X为H元素,据此解答.
解答 解:前四周期元素X、Y、Z、W核电荷数依次增加,Y 原子的M层p轨道有3个未成对电子,则外围电子排布为3s23p3,故Y为P元素;Z与Y同周期,且在该周期中电负性最大,则Z为Cl元素;W原子的L层电子数与最外层电子数之比为4:1,最外层电子数为2,其d轨道中的电子数与最外层电子数之比为5:2,d轨道电子数目为5,外围电子排布为3d54s2,故W为Mn元素,而X、Y、Z、W四种元素的核电荷数之和为58,则X核电荷数为58-15-17-25=1,故X为H元素.
(1)由上述分析可知,Z为Cl元素,在元素周期表中的位置:第三周期第ⅦA族,
故答案为:三;ⅦA;
(2)Y与X形成共价化合物为PH3,P原子形成3个P-H键,含有1对孤对电子,故P原子杂化方式为sp3,分子空间构型为三角锥形,
故答案为:sp3;三角锥形;
(3)Z为Cl元素,最高价氧化物对应水化物为HClO4,故答案为:HClO4;
(4)故W为Mn元素,外围电子排布为3d54s2,价电子排布图为 ,最高正价为+7,
,最高正价为+7,
故答案为: ;+7.
;+7.
点评 本题考查结构性质位置关系应用,推断元素是解题的关键,注意熟练掌握核外电子排布规律,会进行杂化方式与空间构型判断.

 名师点拨卷系列答案
名师点拨卷系列答案| A. | 煤的干馏 | B. | 石油的分馏 | C. | 石油的裂化 | D. | 天然气的燃烧 |
该反应达到平衡状态的标志是( )
| A. | v正(HI)=v逆(I2) | |
| B. | c(HI)=c(H2)=c(I2) | |
| C. | c(H2)、c(I2)、c(HI)保持不变 | |
| D. | 拆开2mol H-I共价键,同时生成1mol H-H |
| A. | SO3和BF3 | B. | SO42-和PO43- | C. | CO2和CNS- | D. | SO32-和CO32- |
| A. | 减少进气量,增大进风量 | B. | 减少进气量,减少进风量 | ||
| C. | 不作任何改变 | D. | 增大进气量,减少进风量 |
 下表给出五种短周期元素的相关信息.
下表给出五种短周期元素的相关信息.| 元素 | 相关信息 |
| A | 常温、常压下,其单质是最轻的气体,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 常温下其单质为黄绿色气体,其单质水溶液有漂白、杀菌作用 |
(1)D元素核外电子排布
 ;
;(2)A、B两元素形成的含有非极性键的化合物的结构式H-O-O-H;A、B两元素形成的具有相同电子数的离子有(填化学式):OH-、H3O+.
(3)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1:2)一起用作火箭助推剂,两者发生反应生成无毒物质,写出上述化学反应方程式:2N2H4+N2O4═3N2+4H2O.
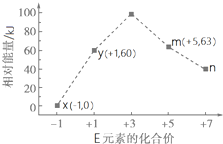
(4)一定条件下,在水溶液中1mol E-、EO${\;}_{x}^{-}$(x=1,2,3,4)的能量(kJ)相对大小如右图所示.n是ClO4-(填离子符号).离子反应y→x+m的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO3-(aq)△H=-117kJ•mol-1(用离子符号表示).
(5)Na2DB3水溶液中各离子浓度的大小顺序是Na+>SO32->OH->HSO3->H+(填离子符号)
| A. | 非金属性强弱:X>Y>Z | B. | 原子序数大小:X<Y<Z | ||
| C. | 原子半径大小:X<Y<Z | D. | 原子最外层电子数:X>Y>Z |
| A. | 除去甲烷中少量的乙炔:通入酸性高锰酸钾溶液,再通入氢氧化钠溶液洗气 | |
| B. | 除去乙烯中少量的乙烷:通入足量溴水中,然后洗气 | |
| C. | 除去乙烷中少量的乙烯:光照条件下通入氯气,然后气液分离 | |
| D. | 除去苯酚中少量的苯:加入足量的氢氧化钠溶液,分液后在通入足量二氧化碳 |