题目内容
13.天然气的主要成分是甲烷,液化气的主要成分是丁烷,欲将烧液化气的灶具改烧天然气,使燃料充分燃烧且灶具温度最高,下列操作正确的是( )| A. | 减少进气量,增大进风量 | B. | 减少进气量,减少进风量 | ||
| C. | 不作任何改变 | D. | 增大进气量,减少进风量 |
分析 丁烷燃烧的化学方程式为:2C4H10+13O2 $\stackrel{点燃}{→}$8CO2+10H2O,甲烷燃烧的化学方程式为:CH4+2O2 $\stackrel{点燃}{→}$CO2+2H2O,根据丁烷和甲烷的燃烧反应可知,等体积的丁烷和甲烷相比,甲烷耗氧量更少,据此分析调整措施.
解答 解:丁烷燃烧的化学方程式为:2C4H10+13O2 $\stackrel{点燃}{→}$8CO2+10H2O,甲烷燃烧的化学方程式为:CH4+2O2 $\stackrel{点燃}{→}$CO2+2H2O,由化学方程式的微观粒子个数比可知,燃烧相同体积的液化石油气和天然气时,天然气消耗的氧气少.燃烧液化石油气的灶具如需改燃天然气,同体积燃料燃烧消耗空气的体积将减小,则灶具的调整方法是增大进气量,或减少进风量,故选D.
点评 本题主要考查燃料的性质和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.能够说明氯的非金属性比硫强的事实有( )
①HCl酸性强于H2S的酸性
②将氯气通入H2S溶液中可置换出硫
③氯气与铁反应生成FeCl3,硫与铁反应生成FeS
④硫和氯变成简单阴离子时硫原子得到的电子更多
⑤氯气和氢气的混合气,经强光照射可剧烈反应,而硫与氢气反应需较高温度.
①HCl酸性强于H2S的酸性
②将氯气通入H2S溶液中可置换出硫
③氯气与铁反应生成FeCl3,硫与铁反应生成FeS
④硫和氯变成简单阴离子时硫原子得到的电子更多
⑤氯气和氢气的混合气,经强光照射可剧烈反应,而硫与氢气反应需较高温度.
| A. | ②③⑤ | B. | ①③⑤ | C. | ①②③ | D. | ①②③⑤ |
4.如图是某课外活动小组设计的用化学电源使LED灯发光的装置.下列说法错误的是( )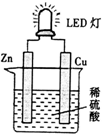

| A. | 铜极反应式为:2H++2e-=H2↑ | |
| B. | 电子从锌片通过溶液流向铜片 | |
| C. | 装置中存在“化学能→电能→光能”的转换 | |
| D. | 如果将锌片换成铁片,电路中的电流方向不变 |
1.下列电子排布式错误的是( )
| A. | 1s22s22p3 | B. | 1s22s22p62d53s1 | C. | [Ar]3d54s1 | D. | [Ar]3d94s1 |
8.下列叙述中错误的是( )
| A. | 乙烯和苯使溴水褪色的原理不同 | |
| B. | 乙烯和聚乙烯中都有碳碳双键 | |
| C. | 煤的气化和液化都是化学变化 | |
| D. | 甲烷中混有乙烯时,仅用酸性KMnO4溶液不能提纯 |
2.为了加快锌与稀硫酸的反应制氢气的速率,下列方法错误的是( )
| A. | 适当提高硫酸浓度 | B. | 将锌粒变小 | ||
| C. | 将硫酸改为浓硫酸 | D. | 适当升高温度 |
3.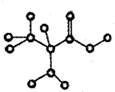 如图是某有机物简易球棍模型,已知它只含有C、H、O、N四种元素,下列关于该有机物的说法正确的是( )
如图是某有机物简易球棍模型,已知它只含有C、H、O、N四种元素,下列关于该有机物的说法正确的是( )
 如图是某有机物简易球棍模型,已知它只含有C、H、O、N四种元素,下列关于该有机物的说法正确的是( )
如图是某有机物简易球棍模型,已知它只含有C、H、O、N四种元素,下列关于该有机物的说法正确的是( )| A. | 分子式为C3H7NO | |
| B. | 不能和NaHCO3溶液反应生成CO2 | |
| C. | 该分子中至少存在5个原子一定共面 | |
| D. | 可以与醇发生酯化反应 |
 ,W的最高正价为+7.
,W的最高正价为+7.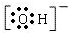 .
.