题目内容
4.下列物质的保存方法正确的是( )| A. | 氢氟酸保存在用塑料塞的玻璃瓶中 | |
| B. | 液溴盛放在用橡胶塞的玻璃瓶中 | |
| C. | 氯水贮存于棕色玻璃瓶中,密闭保存于阴凉处 | |
| D. | 硅酸钠溶液密封保存在玻璃塞的玻璃瓶中 |
分析 A.氢氟酸能和二氧化硅反应;
B.液溴腐蚀橡胶;
C.见光易分解的物质贮存于棕色玻璃瓶中;
D.硅酸钠是黏性的物质.
解答 解:A.氢氟酸腐蚀玻璃,所以不能放在玻璃瓶中,故A错误;
B.液溴腐蚀橡胶,应用玻璃塞,故B错误;
C.氯水中的次氯酸见光易分解而导致氯水变质,应于棕色试剂瓶避光保存,故C正确;
D.硅酸钠是黏性的物质,能把玻璃塞黏住,所以不能盛放在用玻璃塞的玻璃瓶中,故D错误;
故选C.
点评 本题考查了化学试剂的存放,难度不大,要根据试剂的化学性质选取相应的贮存方法.

练习册系列答案
相关题目
15.已知可逆反应a A(g)+b B(?)?c C(g)△H>0(B物质的状态未确定).关于该反应的描述正确的是( )
| A. | 加压若平衡正向移动,则a>c | |
| B. | 加入一定量的B,平衡一定正向移动 | |
| C. | 缩小容器的体积,各物质的浓度一定增大 | |
| D. | 升高温度,平衡一定正向移动,混合气体的平均摩尔质量的变化不能确定 |
12.下列关于硫及其化合物的说法中正确的是( )
| A. | 自然界中不存在游离态的硫 | |
| B. | SO2和SO3都是酸性氧化物,二者的水溶液都是强酸 | |
| C. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 | |
| D. | 将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化 |
19. 请运用化学反应原理的相关知识研究碳及其化合物的性质.
请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g)?CO(g)+H2O(g),平衡常数K与温度t℃的关系如下表:
①该反应的化学平衡常数表达式为$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
②该反应为吸热反应(填“吸热”或“放热”).
③某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(2)工业上一般以CO和H2为原料合成甲醇,一定温度下在恒容容器中,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
①下列措施中能说明反应达到平衡状态的是AD.
A.体系压强保持不变
B.混合气体的密度保持不变
C.CO与H2的浓度之比为1:2
D.单位时间内,消耗2molH2的同时消耗1molCH3OH
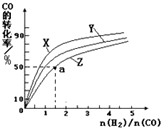
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2):n(CO)的起始组成比的关系如图所示.已知容器体积1L,起始时CO的物质的量均为1mol.据此判断在上述三种温度中,曲线Z对应的温度是270℃;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K等于4(mol/L)-2.
 请运用化学反应原理的相关知识研究碳及其化合物的性质.
请运用化学反应原理的相关知识研究碳及其化合物的性质.(1)在一定体积的密闭容器中,进行如下化学反应,CO2(g)+H2(g)?CO(g)+H2O(g),平衡常数K与温度t℃的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②该反应为吸热反应(填“吸热”或“放热”).
③某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(2)工业上一般以CO和H2为原料合成甲醇,一定温度下在恒容容器中,该反应的热化学方程式为:
CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
①下列措施中能说明反应达到平衡状态的是AD.
A.体系压强保持不变
B.混合气体的密度保持不变
C.CO与H2的浓度之比为1:2
D.单位时间内,消耗2molH2的同时消耗1molCH3OH
②在恒容容器中合成甲醇,当温度分别为230℃、250℃和270℃时,CO的转化率与n(H2):n(CO)的起始组成比的关系如图所示.已知容器体积1L,起始时CO的物质的量均为1mol.据此判断在上述三种温度中,曲线Z对应的温度是270℃;利用图中a点对应的数据,计算该反应在对应温度下的平衡常数K等于4(mol/L)-2.
13.用ωg氢氧化钠配制一定浓度的溶液来滴定盐酸,若氢氧化钠中混有碳酸钠,则测得盐酸的浓度是( )
| A. | 偏高 | B. | 偏低 | C. | 不变 | D. | 无法判断 |
1. 蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
实验步骤如图甲,请回答下列问题:
(1)实验室完成操作①所用到的玻璃仪器有玻璃棒、漏斗、烧杯.
(2)检验溶液Ⅱ中是否含有Fe3+的操作与结论是取少量溶液Ⅱ于试管中,加入KSCN溶液,若无明显现象,说明溶液Ⅱ不含Fe3+;若溶液变红色,说明溶液Ⅱ含有Fe3+
(3)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为OH-+Al(OH)3═AlO2-+2H2O,再进行过滤、洗涤、加热(依次填写实验操作名称).
(4)操作②中应控制溶液pH的合理范围是C(填序号).
A.小于1.5 B.1.5~3.3 C.7~8 D.大于9.4
(5)为探究所得的水合碱式碳酸镁[xMgCO3•yMg(OH)2•zH2O]的组成,取样7.28g于装置A的玻璃管中,请按由左-→右顺序将如图乙装置连接好(填序号,装置可重复使用)C-→B-→A-→B-→D-→B(或D),装置C应盛的试剂是氢氧化钠溶液.充分反应后,如果实验测得硬质玻璃管中剩余固体3.2g,共放出2.64g CO2气体,则x:y:z=3:1:3.
 蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:
蛇纹石可以看作由MgO、Fe2O3、Al2O3、SiO2组成.实验室以蛇纹石为原料制取水合碱式碳酸镁,已知:| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(1)实验室完成操作①所用到的玻璃仪器有玻璃棒、漏斗、烧杯.
(2)检验溶液Ⅱ中是否含有Fe3+的操作与结论是取少量溶液Ⅱ于试管中,加入KSCN溶液,若无明显现象,说明溶液Ⅱ不含Fe3+;若溶液变红色,说明溶液Ⅱ含有Fe3+
(3)从沉淀混合物B中制取D,应加入一种试剂进行分离,其反应的离子方程式为OH-+Al(OH)3═AlO2-+2H2O,再进行过滤、洗涤、加热(依次填写实验操作名称).
(4)操作②中应控制溶液pH的合理范围是C(填序号).
A.小于1.5 B.1.5~3.3 C.7~8 D.大于9.4
(5)为探究所得的水合碱式碳酸镁[xMgCO3•yMg(OH)2•zH2O]的组成,取样7.28g于装置A的玻璃管中,请按由左-→右顺序将如图乙装置连接好(填序号,装置可重复使用)C-→B-→A-→B-→D-→B(或D),装置C应盛的试剂是氢氧化钠溶液.充分反应后,如果实验测得硬质玻璃管中剩余固体3.2g,共放出2.64g CO2气体,则x:y:z=3:1:3.
 ;
;
 2SO3.
2SO3.