题目内容
12.下列关于硫及其化合物的说法中正确的是( )| A. | 自然界中不存在游离态的硫 | |
| B. | SO2和SO3都是酸性氧化物,二者的水溶液都是强酸 | |
| C. | 浓硫酸可用来干燥SO2、CO、Cl2等气体 | |
| D. | 将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化 |
分析 A.自然界中存在硫单质;
B.亚硫酸为弱酸;
C.浓硫酸具有吸水性,与O2、CO、Cl2都不反应;
D.铜与浓硫酸在常温下不反应.
解答 解:A.自然界中存在游离态的硫,故A错误;
B.SO2和SO3都是酸性氧化物,二者的水溶液后者是强酸,前者是弱酸,故B错误;
C.浓硫酸具有吸水性,与O2、CO、Cl2都不反应,可以干燥O2、CO、Cl2,故C正确;
D.将铜片放入浓硫酸中,无明显现象是因为铜片与浓硫酸在常温下不反应,故D错误;
故选:C.
点评 本题考查了硫及其化合物,明确硫在自然界中存在形态、二氧化硫、浓硫酸的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
3.若要除去下列溶液中的杂质(括号内为杂质),请将选用的试剂及有关反应的化学方程式填入下表的空白处:
| 物质(杂质) | 试剂 | 有关化学方程式 |
| NaHCO3(Na2CO3) | CO2 | Na2CO3+H2O+CO2=2NaHCO3 |
| FeCl2(FeCl3) | Fe | 2FeCl3+Fe═3FeCl2 |
20.为测某镁铝合金样品中铝的含量,某实验小组进行了下列实验:取一定量合金,加入100mL0.3mol•L-1稀硫酸,合金完全溶解,产生的气体在标准状况下体积为560mL;再不断滴加0.2mol•L-1NaOH溶液至沉淀质量恰好在此时不再变化,用去350mL NaOH溶液.则所取样品中铝的物质的量为( )
| A. | 0.005mol | B. | 0.01mol | C. | 0.025mol | D. | 0.03mol |
17.下列有关说法正确的是( )
| A. | 吸热反应一定不可以自发进行 | |
| B. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 | |
| C. | NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 | |
| D. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 |
4.下列物质的保存方法正确的是( )
| A. | 氢氟酸保存在用塑料塞的玻璃瓶中 | |
| B. | 液溴盛放在用橡胶塞的玻璃瓶中 | |
| C. | 氯水贮存于棕色玻璃瓶中,密闭保存于阴凉处 | |
| D. | 硅酸钠溶液密封保存在玻璃塞的玻璃瓶中 |
9.某无色溶液能与铝作用放出H2,则下列离子组合中可能的是( )
| A. | H+、Cl-、Cu2+、Ba2+ | B. | OH-、NO${\;}_{3}^{-}$、Ba2+、Cl- | ||
| C. | H+、CO${\;}_{3}^{2-}$、Mg2+、Ba2+ | D. | OH-、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$、Mg2+ |

 ,化合物C所含官能团的名称为羧基.
,化合物C所含官能团的名称为羧基. .
.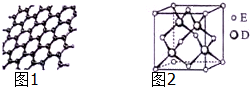 原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
原子序数依次增大的五种元素A、B、C、D、E位于周期表的前四周期.A基态原子的2p轨道上有2个未成对电子;C的最外层电子数是次外层电子数的3倍,C与D同主族相邻;E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题: