题目内容
14.表是元素周期表的一部分,表中的每个字母表示一种短周期元素.回答下列问题:
(1)A的原子结构示意图为
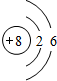 .
.(2)A、B、X、Y、Z五种元素所形成的气体氢化物中,最稳定的是HF(填化学式).
(3)Y元素在周期表中所属的周期和族为第三周期VIA族.
(4)X、Y元素的最高价氧化物对应水化物的酸性较强的是H2SO4.(填化学式)
(5)C和Z形成化合物的电子式为
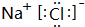 .
.
分析 由元素在短周期中位置,可知A为氧,B为氟,C为Na,D为Al,X为磷,Y为硫,Z为Cl.
(1)氧原子核外电子数为8,结合核外电子排布规律画出原子结构示意图;
(2)元素非金属性越强,对应氢化物越稳定;
(3)由Y的位置可知,处于第三周期VIA族;
(4)非金属性越强,最高价氧化物对应水化物的酸性越强;
(5)C和Z形成化合物为NaCl,由钠离子与氯离子构成.
解答 解:由元素在短周期中位置,可知A为氧,B为氟,C为Na,D为Al,X为磷,Y为硫,Z为Cl.
(1)氧原子核外电子数为8,原子结构示意图为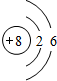 ,故答案为:
,故答案为: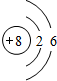 ;
;
(2)A、B、X、Y、Z五种元素中F元素非金属性最强,元素非金属性越强,对应氢化物越稳定,故HF最稳定,故答案为:HF;
(3)由Y的位置可知,处于第三周期VIA族,故答案为:第三周期VIA族;
(4)同周期自左而右非金属性最强,非金属性越强,最高价氧化物对应水化物的酸性越强,故酸性:H2SO4>H3PO4,故答案为:H2SO4;
(5)C和Z形成化合物为NaCl,由钠离子与氯离子构成,电子式为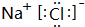 ,故答案为:
,故答案为: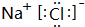 .
.
点评 本题考查元素周期表与元素周期律表的应用,比较基础,熟练掌握前四周期元素,注意对元素周期律理解掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.对于反应A2+B2=2AB来说,下列速率表示该反应最快的是( )
| A. | V(B2)=0.2mol/(L•S) | B. | V(A2)=6mol/(L•min) | ||
| C. | V(AB)=8mol/(L•min) | D. | V(B2)=1.2mol/(L•min) |
6.下列说法不正确的是( )
| A. | 沸点:正戊烷>2-甲基丁烷>丙烷 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 | |
| C. | 相对分子质量相近的醇比烷烃沸点高是因为醇分子间存在氢键 | |
| D. | 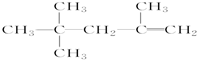 的名称为2,2,4-三甲基-4-戊烯 的名称为2,2,4-三甲基-4-戊烯 |
3.下列有关能源的说法错误的是( )
| A. | 风能是人类通过风车等工具获取的能源,但属于一次能源 | |
| B. | 在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源 | |
| C. | 月球土壤中含有丰富的质量数为3的氦,它可作为未来核能的重要原料 | |
| D. | 原电池把化学能直接转化为电能,所以由原电池提供的电能是一次能源 |
4.化学能与热能、电能等能相互转化.关于化学能与其他能量相互转化的说法正确的是( )

| A. | 化学反应中能量变化的主要原因是物质状态的改变 | |
| B. | 铝热反应中,反应物的总能量比生成物的总能量高 | |
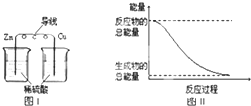
| C. | 图I所示的装置能将化学能转变为电能 | |
| D. | 图II所示的反应为吸热反应 |
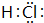 .
.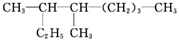 3,4-二甲基辛烷
3,4-二甲基辛烷 ,1mol该烃完全燃烧需消耗氧气18.5mol.
,1mol该烃完全燃烧需消耗氧气18.5mol.