题目内容
17.已知在标况下的四种气体 ①6.72L CH4 ②3.01×1023个HCl分子 ③13.6克H2S④0.2molNH3密度最大的是②(填序号)分析 相同条件下,气体摩尔体积相同,根据ρ=$\frac{M}{{V}_{m}}$可知,气体的摩尔质量越大,其密度越大,据此进行解答.
解答 解:根据ρ=$\frac{M}{{V}_{m}}$可知,相同条件下,气体的摩尔质量越大,其密度越大,四种气体中摩尔质量最大的为②HCl,则密度最大的是②,
故答案为:②.
点评 本题考查了物质的量的计算,题目难度不大,明确相同条件下气体密度与摩尔质量成正比为解答关键,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案
相关题目
7.工业上以沙子为原料制取粗硅,主要反应的化学方程式为2C(s)+SiO2(s)=Si (s)+2CO(g)△H>O,对该反应的说法中不正确的是( )
| A. | △S>0 | |
| B. | 产物CO 为酸性氧化物 | |
| C. | 高温条件下才能自发进行 | |
| D. | 采用碎沙而非石块的原因可能是加快反应速率 |
8.下列说法中正确的是( )
| A. | 羟基和氢氧根离子有相同的化学式和结构式 | |
| B. | 乙醇的官能团是羟基 | |
| C. | NaOH中含有羟基 | |
| D. | 乙醇与钠反应中,羟基被取代 |
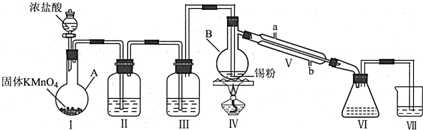
12.实验室里用下列仪器和药品制取纯净的无水氯化铜.根据要求完成以下问题:
(1)按气体从左向右流动,装置②在④左边,则②中加入的液体是饱和食盐水;
(2)装置⑤中发生反应的化学方程式是MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2Cl2↑+2H2O;
(3)实验开始时,应先点燃⑤(填装置序号)处的酒精灯,否则CuCl2中含有CuO(填化学式)杂质.待充分反应后,装置①的玻璃管中剩余物呈棕黄色;
(4)某实验小组组装装置时,在①和⑥之间添加了一个盛有浓硫酸的洗气瓶,其作用是防止氢氧化钠溶液中的水蒸气进入装置①.
| 序号 | ① | ② | ③ | ④ | ③ | ⑥ |
| 仪器及装置图 |  |  |  |  |  |  |
(2)装置⑤中发生反应的化学方程式是MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2Cl2↑+2H2O;
(3)实验开始时,应先点燃⑤(填装置序号)处的酒精灯,否则CuCl2中含有CuO(填化学式)杂质.待充分反应后,装置①的玻璃管中剩余物呈棕黄色;
(4)某实验小组组装装置时,在①和⑥之间添加了一个盛有浓硫酸的洗气瓶,其作用是防止氢氧化钠溶液中的水蒸气进入装置①.
9.下列反应的离子方程式书写正确的是( )
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 稀硫酸与Ba(OH)2溶液混合:SO42-+Ba2+═BaSO4↓ | |
| C. | 稀硝酸滴在大理石上:CaCO3+2H+═Ca2++H2CO3 | |
| D. | 氧化铁与稀盐酸混合:Fe2O3+6H+═2Fe3++3H2O |
6.“纳米材料”是指直径在几纳米到几十纳米的材料.如将“纳米材料”分散到液体分散剂中,所得混合物具有的性质是( )
| A. | 能全部透过半透膜 | B. | 所得物质一定为悬浊液或乳浊液 | ||
| C. | 所得混合物一定能导电 | D. | 有丁达尔效应 |
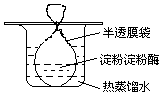 把一定量的淀粉和少量淀粉酶配成溶胶灌于半透膜袋中并置于盛有热的蒸馏水的烧杯中(如图所示).一段时间后进行如下实验,回答相关问题.
把一定量的淀粉和少量淀粉酶配成溶胶灌于半透膜袋中并置于盛有热的蒸馏水的烧杯中(如图所示).一段时间后进行如下实验,回答相关问题.