��Ŀ����
20����X��Y��Z��T��W���ֶ�����Ԫ�أ�ԭ��������������X��Tͬ���壬��XԪ��������Ԫ�ز���ͬһ���ڣ�Y��Z��ͬ�����д�������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壮Wԭ�ӵ������������Ǻ�����Ӳ�����2������ش���1��W�����ڱ��е�λ��Ϊ�������ڢ�A�壮
��2��д��X��Z�γɵ�10���������ӵĻ�ѧʽH3O+��
��3��W��һ�����������Ư���ԣ���ҵ����Y����̬�⻯���ˮ��Һ�������ռ���д�����ռ������������ﷴӦ�����ӷ���ʽSO2+NH3•H2O�THSO3-+NH4+��
��4��������T2Z2�����Ļ�ѧ�������Ӽ������ۼ��������ʽΪ
 ��
����5��19.2g��ͭ��������Y������������ˮ�������Һ��Ӧ�������õ�������3.36L O2����״���£���ϣ�ǡ���ܱ�ˮ��ȫ���գ�
���� ��X��Y��Z��T��W���ֶ�����Ԫ�أ�ԭ��������������Y��Z��ͬ�����д�������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壬��YΪNԪ�ء�ZΪOԪ�أ�Wԭ�ӵ������������Ǻ�����Ӳ�����2����ԭ��������������ֻ�ܴ��ڵ������ڣ�����������Ϊ6����WΪSԪ�أ�XԪ��������Ԫ�ز���ͬһ���ڣ���XΪHԪ�أ�X��Tͬ���壬T��ԭ����������������TΪNa���ݴ˽��
��� �⣺��X��Y��Z��T��W���ֶ�����Ԫ�أ�ԭ��������������Y��Z��ͬ�����д�������λ�ã����ǵĵ�����ͨ��״���¾�Ϊ��ɫ���壬��YΪNԪ�ء�ZΪOԪ�أ�Wԭ�ӵ������������Ǻ�����Ӳ�����2����ԭ��������������ֻ�ܴ��ڵ������ڣ�����������Ϊ6����WΪSԪ�أ�XԪ��������Ԫ�ز���ͬһ���ڣ���XΪHԪ�أ�X��Tͬ���壬T��ԭ����������������TΪNa��
��1��WΪSԪ�أ���Ԫ�����ڱ�λ�ã��������ڢ�A�壬�ʴ�Ϊ���������ڢ�A�壻
��2��H��O�γɵ�10����������ΪH3O+���ʴ�Ϊ��H3O+��
��3��W��һ�����������Ư���ԣ���������ΪSO2����ҵ����Y����̬�⻯�ﰱ����ˮ��Һ�������ռ������ռ������������ﷴӦ�����ӷ���ʽ��SO2+NH3•H2O�THSO3-+NH4+��
�ʴ�Ϊ��SO2+NH3•H2O�THSO3-+NH4+��
��4��������Na2O2�����Ļ�ѧ���У����Ӽ������ۼ��������ʽΪ ���ʴ�Ϊ�����Ӽ������ۼ���
���ʴ�Ϊ�����Ӽ������ۼ��� ��
��
��5��Cu�����ᷴӦ�õ�����������������������������ǡ���ܱ�ˮ��ȫ���գ���Ӧ�ֵõ����ᣬ�ݹ��������̣�Cuʧȥ���ӵ���������õĵ��ʣ�Cu�����ʵ���Ϊ$\frac{19.2g}{64g/mol}$=0.3mol�����ݵ���ת���غ㣬��֪�������ʵ���Ϊ$\frac{0.3mol��2}{4}$=0.15mol���ʱ�����������Ϊ0.15mol��22.4L/mol=3.36L��
�ʴ�Ϊ��3.36��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ�����4����ע�����õ���ת���غ����Ѷ��еȣ�

| A�� | �����ԣ�Na��Mg��Al | B�� | ��һ�����ܣ�Na��Mg��Al | ||
| C�� | �縺�ԣ�Na��Mg��Al | D�� | ���ԣ�NaOH��Mg��OH��2��Al��OH��3 |
| A�� | CCl4��ˮ | B�� | AgCl����Һ | C�� | �Ȼ�����ˮ | D�� | �ƾ���ˮ |
| A�� | Na2O2ʹ��ɫ������ɫ | B�� | ��ˮʹ��ɫ������ɫ | ||
| C�� | ����̿ʹ��īˮ��ɫ | D�� | Ư��ʹijЩȾ����ɫ |
| A�� | ��SO2Ư��ֽ���Ͳ�ñ�� | |
| B�� | �������ý�̿��ԭSiO2��ȡ�ֹ� | |
| C�� | ��������ϴ��¯�е�ˮ�� | |
| D�� | ��Na2S������������ȥ��ˮ�й���Hg2+ |
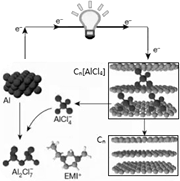 ���������һ�����Ϳɳ��ʽ����أ������Ϊ�����ӣ�EMl+���������ӣ�AlCl4-����ɵ�����Һ�壮ͼΪ�õ�طŵ����ʾ��ͼ��CnΪʯīϩ������˵����ȷ���ǣ�������
���������һ�����Ϳɳ��ʽ����أ������Ϊ�����ӣ�EMl+���������ӣ�AlCl4-����ɵ�����Һ�壮ͼΪ�õ�طŵ����ʾ��ͼ��CnΪʯīϩ������˵����ȷ���ǣ�������| A�� | ���ʱ��ÿ����1mol Al���������Һ�л�����7molAlCl4- | |
| B�� | ���ʱ��CnΪ�������缫����ʽΪCn+AlCl4--e-�TCn[AlCl4] | |
| C�� | �ŵ�ʱ��������Ӧ����ʽΪAl+7AlCl4--3e-�T4Al2Cl7- | |
| D�� | �ŵ�ʱ��������е������ӣ�EMl+���ᷢ����Ӧ |
| A�� | 0.3molHNO3 | B�� | 0.1mol H3PO4 | ||
| C�� | 0.2molCH4 | D�� | 3.612��1023��HCl���� |
