题目内容
8.不用碳酸钠稀溶液除去CO2中混有的少量HCl气体的原因是(用离子方程式表示)CO2+H2O+CO32-=2HCO3-.分析 二者均与碳酸钠反应,不能使用碳酸钠溶液除去,应选碳酸氢钠溶液,以此来解答.
解答 解:不用碳酸钠稀溶液除去CO2中混有的少量HCl气体,发生CO2+H2O+CO32-=2HCO3-,将原物质除去,
故答案为:CO2+H2O+CO32-=2HCO3-.
点评 本题考查离子反应方程式的书写,为高频考点,把握物质的性质、发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意除杂的原则,题目难度不大.

练习册系列答案
相关题目
18.只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、(NH4)2SO4五种溶液,这种试剂是( )
| A. | Ba(OH)2 | B. | H2SO4 | C. | NaOH | D. | Fe(OH)3胶体 |
16.下列做法不能达到实验目的是( )
| A. | 用闻气味的方法鉴别氢气和氧气 | B. | 用氯化钡溶液鉴别盐酸和稀硫酸 | ||
| C. | 观察气体颜色区别氯气和氧气 | D. | 利用丁达尔效应区别溶液和胶体 |
3.下列关于硫酸性质的描述中,正确的是( )
| A. | 浓H2SO4有强氧化性,稀H2SO4完全没有氧化性 | |
| B. | 由于浓H2SO4具有脱水性,所以可用做干燥剂 | |
| C. | 稀硫酸不与铜反应,但把Cu片放在浓H2SO4中立即发生激烈反应 | |
| D. | 在受热的情况下浓硫酸也能与铁、铝发生反应 |
17.下列有关化学研究的正确说法是( )
| A. | 同时改变两个变量来研究反应速率的变化,能更快得出有关规律 | |
| B. | 从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律 | |
| C. | 决定化学反应速率的最主要因素:反应物自身的性质 | |
| D. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
18.下列叙述中,正确的是( )
| A. | 硫酸的摩尔质量是98g | |
| B. | 1 mol H2O的质量为18g/mol | |
| C. | 摩尔是物质的量的单位 | |
| D. | 标准状况下,1 mol任何物质体积均为22.4L |
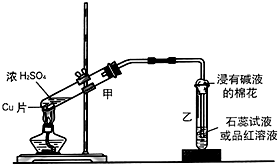 实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验.
实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验. .
.