题目内容
下列与实验相关的叙述正确的是( )
| A、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| B、某溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝的气体,说明原溶液中一定存在NH4+ |
| C、某溶液加入BaCl2溶液,产生了白色沉淀,再加入足量的HNO3溶液,沉淀不溶解,则溶液中一定含有SO42- |
| D、验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银的硝酸溶液,有白色沉淀出现,证明含Cl- |
考点:配制一定物质的量浓度的溶液,常见阳离子的检验,常见阴离子的检验
专题:实验评价题
分析:A、容量瓶是准确而配制准确体积和浓度的量具加水超出刻度线,需要重新配制;
B、能使湿润的红色石蕊试纸变蓝的气体为氨气;
C、BaCl2溶液与硝酸银可以生成氯化银白色沉淀;
D、验证烧碱溶液中是否含有Cl一,加稀盐酸除去OH-,会引入氯离子,造成干扰.
B、能使湿润的红色石蕊试纸变蓝的气体为氨气;
C、BaCl2溶液与硝酸银可以生成氯化银白色沉淀;
D、验证烧碱溶液中是否含有Cl一,加稀盐酸除去OH-,会引入氯离子,造成干扰.
解答:
解:A、配制溶液时,若加水超过容量瓶刻度,溶液浓度变稀,需要重新配制,故A错误;
B、一种未知溶液滴加NaOH溶液,加热后产生能使湿润的红色石蕊试纸变蓝的气体,该气体为氨气,故原溶液中存在铵根,故B正确;
C、BaCl2溶液与硝酸银可以生成氯化银白色沉淀,故此沉淀不一定是硫酸钡,故C错误,
D.验证烧碱溶液中是否含有Cl一,加稀盐酸除去OH-,会引入氯离子,造成干扰,所以验证烧碱溶液中是否含有Cl一,先加稀硝酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含C1-,故D错误;
故选B.
B、一种未知溶液滴加NaOH溶液,加热后产生能使湿润的红色石蕊试纸变蓝的气体,该气体为氨气,故原溶液中存在铵根,故B正确;
C、BaCl2溶液与硝酸银可以生成氯化银白色沉淀,故此沉淀不一定是硫酸钡,故C错误,
D.验证烧碱溶液中是否含有Cl一,加稀盐酸除去OH-,会引入氯离子,造成干扰,所以验证烧碱溶液中是否含有Cl一,先加稀硝酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含C1-,故D错误;
故选B.
点评:本题考查了物质性质的分析判断,注意离子检验时干扰离子的分析,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
已知1-18号元素的离子aW3+、bX+、CY2-、dZ-都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A、四种元素位于同一周期 |
| B、氢化物的稳定性H2Y>HZ |
| C、离子的氧化性aW3+>bX+ |
| D、原子半径Z>Y |
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1),下列说法错误的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的平衡浓度(mol?L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
| A、2c1<c3 |
| B、a+b=92.4 |
| C、a1+a3<1 |
| D、p3>2p2=2p1 |
下列家庭化学小实验不能达到预期目的是( )
| A、食醋(含CH3COOH)可以用来洗涤热水瓶胆中的污垢[含CaCO3、Mg(OH)2] |
| B、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
| C、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| D、用灼烧方法鉴别纯毛线和棉布 |
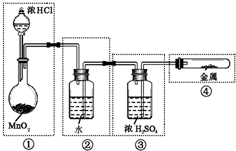 实验室用MnO2与浓HCl反应制Cl2,若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属镁粉的反应.每个虚线框表示一个单元装置,其中错误的是( )
实验室用MnO2与浓HCl反应制Cl2,若用如图所示的实验装置来制备纯净、干燥的氯气,并试验它与金属镁粉的反应.每个虚线框表示一个单元装置,其中错误的是( )| A、只有①和②处 |
| B、只有②处 |
| C、只有①、②和③处 |
| D、①、②、③、④处 |
下列实验操作正确的是( )
A、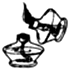 点燃酒精灯 |
B、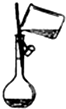 向溶液瓶中转移液体 |
C、 读取液体体积 |
D、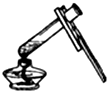 加热液体 |
下列有关说法正确的是( )
| A、塑料垃圾可直接露天焚烧 |
| B、实施“禁塑令”有助于遏制白色污染 |
| C、纤维素、油脂、蛋白质均属于有机高分子 |
| D、聚丙烯结构简式为:-[CH2-CH2-CH2]n- |
