题目内容
现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了确定四种溶液各是什么,将它们随意编上A、B、C、D后,产生的现象如下表所示.根据实验现象按要求回答:
(1)A、B、C、D溶液中溶质的化学式:
A ;B ;C ;D ;
(2)写出上述实验中②③的离子方程式
② ;③ .
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有现象发生 |
| ② | B+D | 有气体放出 |
| ③ | B+C | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
A
(2)写出上述实验中②③的离子方程式
②
考点:无机物的推断
专题:
分析:B和D有气体生成,只有碳酸钠和盐酸反应能生成气体,所以B和D是盐酸和碳酸钠,A和C是氯化钙和硝酸银;A和B没有现象发生,二者应是盐酸与氯化钙,所以B是盐酸,A是氯化钙,则D是碳酸钠,C是硝酸银,据此解答.
解答:
解:B和D有气体生成,只有碳酸钠和盐酸反应能生成气体,所以B和D是盐酸和碳酸钠,A和C是氯化钙和硝酸银;A和B没有现象发生,二者应是盐酸与氯化钙,所以B是盐酸,A是氯化钙,则D是碳酸钠,C是硝酸银,
(1)由上述分析可知,A为CaCl2,B为HCl,C为AgNO3,D为Na2CO3,
故答案为:CaCl2;HCl;AgNO3;Na2CO3;
(2)反应②是盐酸与碳酸钠反应生成氯化钠、水与二氧化碳,反应离子方程式为:CO3 2-+2 H+═CO2↑+H2O;
反应③是盐酸与硝酸银反应生成氯化银与硝酸,反应离子方程式为:Ag++Cl-═AgCl↓,
故答案为:CO3 2-+2 H+═CO2↑+H2O;Ag++Cl-═AgCl↓.
(1)由上述分析可知,A为CaCl2,B为HCl,C为AgNO3,D为Na2CO3,
故答案为:CaCl2;HCl;AgNO3;Na2CO3;
(2)反应②是盐酸与碳酸钠反应生成氯化钠、水与二氧化碳,反应离子方程式为:CO3 2-+2 H+═CO2↑+H2O;
反应③是盐酸与硝酸银反应生成氯化银与硝酸,反应离子方程式为:Ag++Cl-═AgCl↓,
故答案为:CO3 2-+2 H+═CO2↑+H2O;Ag++Cl-═AgCl↓.
点评:本题考查无机物推断、物质的检验,难度不大,注意根据反应现象进行推断,明确复分解反应的条件.

练习册系列答案
相关题目
下列实验操作或叙述中正确的是( )
| A、蒸发操作时,应使混合物中的水分完全蒸干后再停止加热 |
| B、蒸馏时,温度计水银球需靠近蒸馏烧瓶支管口,冷凝水的流向需从冷凝管的上口进下口流出 |
| C、过滤后洗涤沉淀时,应将固体转移至烧杯中,并加入适量蒸馏水充分搅拌后再过滤 |
| D、分液时,先从分液漏斗下口放出下层液体,更换烧杯后再从上口放出上层液体 |
下列实验操作或装置正确的是( )
A、 制取氧气时选用装置 |
B、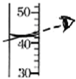 量筒的度数 |
C、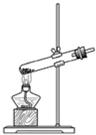 高锰酸钾制取氧气 |
D、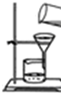 过滤 |
下列与实验相关的叙述正确的是( )
| A、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| B、某溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝的气体,说明原溶液中一定存在NH4+ |
| C、某溶液加入BaCl2溶液,产生了白色沉淀,再加入足量的HNO3溶液,沉淀不溶解,则溶液中一定含有SO42- |
| D、验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银的硝酸溶液,有白色沉淀出现,证明含Cl- |
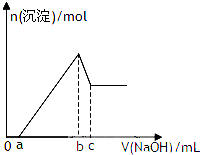 某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、NH4+、Cl-、SO42-、NO3-中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加人NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )
某无色透明酸性溶液,可能含有K+、Mg2+、Al3+、Cu2+、NH4+、Cl-、SO42-、NO3-中的几种,取该溶液三等份分别进行实验①加入少量Zn产生H2,②逐滴加人NaOH溶液,其加入量和沉淀生成量关系如图所示,③加入0.1mol/LBaCl2溶液至5ml时不再产生白色沉淀,取上层清液加入足量AgNO3溶液,得到0.287g沉淀,由此推知原溶液中( )| A、一定没有Cu2+、NO3-、Cl- |
| B、可能有K+、NH4+、NO3-、SO42- |
| C、不能确定是否含有K+、NO3- |
| D、一定有Mg2+、Al3+、Cl-、SO42- |
向盛有I2水溶液的试管中,再加四氯化碳振荡,静置后观察到的现象是( )
| A、上层橙红色,下层接近无色 |
| B、均匀、透明、紫红色 |
| C、均匀、透明、无色 |
| D、上层接近无色,下层紫红色 |
下列物质可通过化合反应直接制得到的是( )
| A、Cu(OH)2 |
| B、Ba(OH)2 |
| C、H2SiO3 |
| D、H2SO4 |
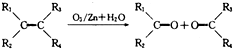 (其中R、R1、R2、R3和R4均表示烃基)今有A~K等11种不同的有机物,它们之间的转化关系如下.其中A为烃,1mol A可得2mol B.
(其中R、R1、R2、R3和R4均表示烃基)今有A~K等11种不同的有机物,它们之间的转化关系如下.其中A为烃,1mol A可得2mol B.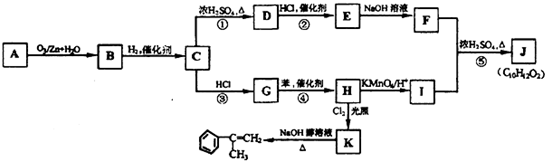
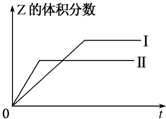 (1)已知:2SO3(g)?2SO2(g)+O2(g),在起始时体积相同的容器A和B中同时分别充入2mol SO3(两容器装有催化剂).在反应过程中,A保持温度和容积不变;B保持温度和压强不变.回答下列问题:
(1)已知:2SO3(g)?2SO2(g)+O2(g),在起始时体积相同的容器A和B中同时分别充入2mol SO3(两容器装有催化剂).在反应过程中,A保持温度和容积不变;B保持温度和压强不变.回答下列问题: